
Wetenschap
Wat zijn de bronnen van fouten in experiment Bepaal enthalpieverandering Hydratatie koper II sulfaat zes?
1. Warmteverlies/winst:
* isolatie: De gebruikte calorimeter is zelden perfect geïsoleerd, waardoor warmte -uitwisseling met de omgeving mogelijk is. Dit kan leiden tot een onnauwkeurige meting van de temperatuurverandering.
* Warmtecapaciteit van de calorimeter: De calorimeter zelf absorbeert wat warmte tijdens de reactie, waardoor de eindtemperatuur wordt beïnvloed. Dit effect wordt vaak genegeerd, wat leidt tot fouten.
* roeren: Krachtig roeren kan warmte door wrijving introduceren, wat de temperatuurlezing beïnvloedt.
2. Meetfouten:
* Temperatuurmetingen: Thermometers hebben beperkingen in nauwkeurigheid, en ze precies lezen kan een uitdaging zijn.
* Massa meting: De nauwkeurigheid van de balans die wordt gebruikt om de chemicaliën te wegen, heeft direct invloed op de berekende enthalpiewijziging.
* Volumemeting: Als het gebruikte volume water niet nauwkeurig wordt gemeten, wordt de berekende enthalpiewijziging beïnvloed.
3. Oplossingsproces:
* Onvolledige ontbinding: Als het koper (II) sulfaat pentahydraat niet volledig oplossen, zal de gemeten enthalpieverandering lager zijn dan de werkelijke waarde.
* Oplossingswarmte: De enthalpieverandering van hydratatie is een specifieke waarde, maar het experiment meet de algehele warmteverandering, inclusief de warmte van oplossing van koper (II) sulfaat. Dit introduceert een fout als de oplossingwarmte niet wordt verantwoord.
* nevenreacties: Sommige koper (II) sulfaat pentahydraat zou kunnen reageren met het water, wat leidt tot een nevenreactie en de waargenomen enthalpieverandering beïnvloeden.
4. Veronderstellingen en benaderingen:
* Constante specifieke warmtecapaciteit: Het experiment veronderstelt vaak dat de specifieke warmtecapaciteit van de oplossing constant is, wat een benadering is. De specifieke warmtecapaciteit kan enigszins variëren, afhankelijk van de concentratie van de oplossing.
* Ideale omstandigheden: De berekening veronderstelt ideale omstandigheden, het verwaarlozen van factoren zoals warmteverlies, onvolledige oplossing en nevenreacties.
5. Andere factoren:
* zuiverheid van chemicaliën: Onzuiverheden in de chemicaliën kunnen de reactie en enthalpieverandering aanzienlijk beïnvloeden.
* luchtbellen: Als luchtbellen vastzitten in de calorimeter, kunnen ze de warmteoverdracht verstoren en de temperatuurwaarden beïnvloeden.
Fouten minimaliseren:
* Verbeter isolatie: Gebruik een goed geïsoleerde calorimeter of voer het experiment uit in een gecontroleerde omgeving.
* Vergelijk voor warmtecapaciteit: Gebruik een correctiefactor voor de warmtecapaciteit van de calorimeter.
* Kalibreerapparatuur: Kalibreer de thermometer en balans om nauwkeurige metingen te garanderen.
* Zorg voor volledige ontbinding: Gebruik voldoende water en roer goed om ervoor te zorgen dat het koper (II) sulfaat pentahydraat volledig oplost.
* Controle roeren: Gebruik een consistente roersnelheid gedurende het experiment om wrijvingswarmte te minimaliseren.
* Gebruik hoge chemicaliën met hoge zuiverheid: Zorg ervoor dat de gebruikte chemicaliën van hoge zuiverheid zijn om de impact van onzuiverheden te verminderen.
Door de potentiële bronnen van fouten te begrijpen en geschikte technieken te implementeren om ze te minimaliseren, kunt u nauwkeurigere en betrouwbare resultaten verkrijgen voor de enthalpiewijziging van de hydratatie van koper (II) sulfaat pentahydraat.
 Hoe heet een relatief lage opgeloste concentratie?
Hoe heet een relatief lage opgeloste concentratie?  Welke twee stikstofbases zijn gebonden door drie waterstofbruggen?
Welke twee stikstofbases zijn gebonden door drie waterstofbruggen?  Zal de NH3 de afname of geen verandering in de pH toenemen wanneer toegevoegd aan water?
Zal de NH3 de afname of geen verandering in de pH toenemen wanneer toegevoegd aan water?  Wereldwijd gebruikte angstdrug tegen lage kosten uit afvalwater verwijderen
Wereldwijd gebruikte angstdrug tegen lage kosten uit afvalwater verwijderen Hoe verhoogt u het aantal botsingen tussen moleculen?
Hoe verhoogt u het aantal botsingen tussen moleculen?
 Kan 'cocktailgeo-engineering' het klimaat redden?
Kan 'cocktailgeo-engineering' het klimaat redden?  Wat hebben Australië en Antarctica gemeen?
Wat hebben Australië en Antarctica gemeen?  Het offshore boorplan van Trump ligt mogelijk dood in het water maar er zijn betere manieren om te leiden op energie
Het offshore boorplan van Trump ligt mogelijk dood in het water maar er zijn betere manieren om te leiden op energie De cryosfeer van de aarde krimpt met 87, 000 vierkante kilometer per jaar
De cryosfeer van de aarde krimpt met 87, 000 vierkante kilometer per jaar Levenscyclus van een pauw
Levenscyclus van een pauw
Hoofdlijnen
- Wat is de volgorde van een DNA -stam?
- Zeewier bevat veel vitamines en mineralen, maar dat is niet de enige reden waarom westerlingen er meer van zouden moeten eten
- Wat is er verschillend tussen organisme en egucatie?
- Onderzoekers vinden eerste wilde alligator brekende schildpad in Illinois sinds 1984
- Sommige mariene soorten zijn kwetsbaarder voor klimaatverandering dan andere
- Vergelijk en contrasteer de structuur van de dierlijke cel van de plant die aangeeft welke organellen uniek zijn voor elk ook in beide?
- Waar remmen cycloheximide eiwitsynthese?
- Wat is de rol van isolatie in evolutie?
- Welke takken van de natuurwetenschap omvatten de studie een organisme dat 10 miljoen jaar geleden leefde?
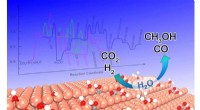
- Water zou de activiteit en selectiviteit van koolstofdioxidereductie kunnen moduleren
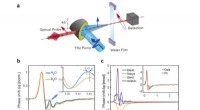
- Ultrasnelle waterstofbrugdynamiek van vloeibaar water onthuld door THz-geïnduceerd Kerr-effect
- Chemici gebruiken licht om biologisch actieve verbindingen te bouwen

- Draagbaar apparaat verlicht de weg naar betere detectie van door voedsel overgedragen ziekten

- Adsorberen of niet adsorberen? Dat is de vraag

 Kan energie worden vernietigd en gecreëerd?
Kan energie worden vernietigd en gecreëerd?  Hoe bedenken geologen rock-layer puzzels?
Hoe bedenken geologen rock-layer puzzels?  Hoe het uitwisselingsprincipe van Locard werkt
Hoe het uitwisselingsprincipe van Locard werkt  Wie plaatst de sterren in de lucht volgens de Griekse mythologie?
Wie plaatst de sterren in de lucht volgens de Griekse mythologie?  Hoe kunnen indexfossielen ons helpen erachter te komen hoe de continenten vroeger werden gerangschikt?
Hoe kunnen indexfossielen ons helpen erachter te komen hoe de continenten vroeger werden gerangschikt?  Hoe noemen we 2 oplossingen die hetzelfde waterpotentieel hebben?
Hoe noemen we 2 oplossingen die hetzelfde waterpotentieel hebben?  Wat is de lengte van de dag op elk zonnesysteem van planeten?
Wat is de lengte van de dag op elk zonnesysteem van planeten?  Halfgeleidend grafeen:fabricage op siliciumcarbide met patroon produceert bandgap om grafeenelektronica te bevorderen
Halfgeleidend grafeen:fabricage op siliciumcarbide met patroon produceert bandgap om grafeenelektronica te bevorderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

