
Wetenschap
Welke heeft een hogere dissociatie constante NaCl of Ch3coona?
Dit is waarom:
* NaCl is een zout van een sterk zuur (HCL) en een sterke basis (NaOH). Het dissocieert volledig in water, wat betekent dat het bijna volledig in zijn ionen (Na⁺ en Cl⁻) afbreekt. Dit betekent dat de Kₐ extreem hoog is, praktisch oneindig.
* ch₃coona is een zout van een zwak zuur (ch₃cooh, azijnzuur) en een sterke basis (NaOH). Het ondergaat gedeeltelijke hydrolyse, wat betekent dat het niet volledig in water dissocieert. Het acetaation (ch₃coo⁻) reageert met water om azijnzuur (ch₃cooh) en hydroxide -ionen te vormen (oh⁻). Deze reactie resulteert in een lagere Kₐ vergeleken met NaCl.
Sleutelpunt: De dissociatieconstante is een maat voor de mate waarin een verbinding in oplossing dissocieert. Zouten van zwakke zuren en sterke basen hebben hogere Kₐ -waarden dan zouten van sterke zuren en sterke basen.
Hoofdlijnen
- Anti-insuline-eiwit gekoppeld aan levensduur en voortplanting bij mieren
- Moet je biologie en chemie of psychologie studeren om een dierenverpleegkundige te worden?
- Wat is een echovrije cyste?
- Wat is het kenmerk van een celmembraan dat regelt welke stoffen cel kunnen binnenkomen en verlaten?
- Wat is de studie van hoe een interne structuur van een organismen functioneert?
- Waarom heeft het Digestif -systeem meer organen?
- Kan mRNA een dubbele streng zijn?
- Als u een adenine vindt op een sporten DNA met welke basis wordt deze verbonden?
- geproduceerd door het lichaam om u te helpen beschermen tegen ziekten?
- Atomair gedispergeerd Ni is cokesbestendig voor droge reforming van methaan

- Nieuwe methode om mineralen te analyseren onder terrestrische en Martiaanse atmosferische omstandigheden

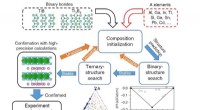
- Een speld in een hooiberg vinden:ontdekking van Ti2InB2 voor het synthetiseren van gelaagde TiB
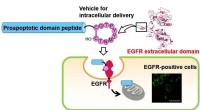
- Ontdekking van een nieuw voertuigpeptide opent een route voor medicijnafgifte
- Algen als levende biokatalysatoren voor een groene industrie

 Waarom zou de wrijving in de poelmassa van touw en rotatie -traagheid allemaal klein zijn?
Waarom zou de wrijving in de poelmassa van touw en rotatie -traagheid allemaal klein zijn?  Hoe bosbranden wijn bederven:vorming van ongewenste aroma's in wijn uitgelegd
Hoe bosbranden wijn bederven:vorming van ongewenste aroma's in wijn uitgelegd Moeders die kinderopvang krijgen van grootouders van moederskant tonen meer ouderlijke warmte, zo blijkt uit onderzoek
Moeders die kinderopvang krijgen van grootouders van moederskant tonen meer ouderlijke warmte, zo blijkt uit onderzoek  Welke vorm van energie wordt geproduceerd wanneer handen samen worden gewreven?
Welke vorm van energie wordt geproduceerd wanneer handen samen worden gewreven?  Welke suiker aanwezig in DNA?
Welke suiker aanwezig in DNA?  Hoe verschilt de levenswetenschap en de aarde?
Hoe verschilt de levenswetenschap en de aarde?  De helderste sterren in dit sterrenbeeld vorm m of een w?
De helderste sterren in dit sterrenbeeld vorm m of een w?  Een gids voor het jagen op zombiesterren
Een gids voor het jagen op zombiesterren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


