
Wetenschap
Welke elementen of moleculen zijn kationen?
1. Elementen:
* metalen: De meeste metalen verliezen meestal elektronen en worden kationen.
* niet -metalen: Sommige niet -metalen kunnen ook kationen vormen, maar dit komt minder vaak voor.
2. Moleculen:
* Polyatomische ionen: Dit zijn groepen atomen die aan elkaar zijn verbonden die een netto positieve lading hebben. Voorbeelden zijn:
* Ammoniumion (NH₄⁺)
* Hydronium -ion (H₃o⁺)
Belangrijke opmerking:
* De lading van een kation wordt bepaald door het aantal verloren elektronen.
* Een natriumatoom (NA) verliest bijvoorbeeld één elektron om een natriumkation (Na⁺) te worden, terwijl een magnesiumatoom (mg) twee elektronen verliest om een magnesiumkation te worden (mg²⁺).
Voorbeelden van kationen:
* Natriumion (Na⁺)
* calciumion (ca²⁺)
* ijzer (ii) ion (fe²⁺)
* aluminium ion (al³⁺)
* koper (i) ion (cu⁺)
* ammoniumion (NH₄⁺)
* hydroniumion (h₃o⁺)
Vergeet niet dat kationen essentiële componenten zijn van ionische verbindingen, waarbij ze elektrostatische bindingen vormen met negatief geladen anionen (ionen met negatieve ladingen).
 Sommige zeedieren zijn mogelijk beter bestand tegen ruwere oceaanomstandigheden dan verwacht
Sommige zeedieren zijn mogelijk beter bestand tegen ruwere oceaanomstandigheden dan verwacht Klimaatverandering een stap voor zijn
Klimaatverandering een stap voor zijn Olympische skiërs en snowboarders strijden op 100% nepsneeuw:heeft dit invloed op de prestaties?
Olympische skiërs en snowboarders strijden op 100% nepsneeuw:heeft dit invloed op de prestaties? Belang van de oostelijke woestijn in het oude Egypte
Belang van de oostelijke woestijn in het oude Egypte Hoe maken natuurbeschermers gebruik van stroomgebieden en ecozones?
Hoe maken natuurbeschermers gebruik van stroomgebieden en ecozones?
Hoofdlijnen
- Kunnen biologische gewassen concurreren met de industriële landbouw?
- Welk deel van de plantencel geeft het vorm en ondersteuning?
- Wat zorgt ervoor dat vliegen aanvallen?
- Welke soorten organismen zijn essentieel voor de koolstofcyclus?
- De kans op gemengd fokken tussen twee zangvogelsoorten neemt af met warmere bronnen
- Wat ervoor zorgt dat vissen seksueel actief worden
- Honingbijen steken minder snel in grotere groepen
- Wat doet het RESTPotory -systeem?
- Wat is een niet -voorbeeld van microscoop?
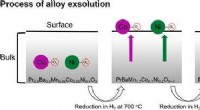
- Hoogwaardige zelf-geassembleerde katalysator voor SOFC
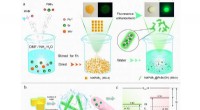
- Loodhalogenide perovskieten met verbeterde luminescentie en stabiliteit
- Ion biljart cue nieuwe materiaal synthese methode

- Materiaalchemici tappen lichaamswarmte af om slimme kleding van stroom te voorzien

- Onderzoekers tonen aan dat zelfsteriliserende polymeren werken tegen SARS-CoV-2
 Wat is het verschil tussen een reactie zonder enzym en met enzym?
Wat is het verschil tussen een reactie zonder enzym en met enzym?  Wat is de geografische reden voor de vorming van Shivalik Range?
Wat is de geografische reden voor de vorming van Shivalik Range?  Sterkere gebouwen kunnen de vernietiging van natuurbranden vertragen, maar niet stoppen, professor zegt
Sterkere gebouwen kunnen de vernietiging van natuurbranden vertragen, maar niet stoppen, professor zegt Onderzoekers onthullen hoe mycorrhiza-soorten de koolstof in de plantenbodem in bossen reguleren
Onderzoekers onthullen hoe mycorrhiza-soorten de koolstof in de plantenbodem in bossen reguleren  Welke maat voor elektrische energieoverdrachten door elektronen in een circuit?
Welke maat voor elektrische energieoverdrachten door elektronen in een circuit?  Hoe beïnvloedt de zon de aarde?
Hoe beïnvloedt de zon de aarde?  Welke wetenschapscategorie zijn rotsen en mineralen?
Welke wetenschapscategorie zijn rotsen en mineralen?  Families die op hun tong bijten om Brexit-ruzies te vermijden, uit onderzoek blijkt
Families die op hun tong bijten om Brexit-ruzies te vermijden, uit onderzoek blijkt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

