
Wetenschap
Wat is de vergelijking voor de reactie van CACL2 met soap natriumoleaat en wat het in balans heeft?
Hier is de onevenwichtige vergelijking:
cacl₂ (aq) + c₁₇h₃₅coona (aq) → (c₁₇h₃₅coo) ₂ca (s) + NaCl (aq)
Om de vergelijking in evenwicht te brengen:
1. Tel het nummer van elk atoom aan beide zijden:
* CA:1 aan de linkerkant, 1 rechts
* CL:2 aan de linkerkant, 1 rechts
* C:17 aan de linkerkant, 34 rechts
* H:35 aan de linkerkant, 70 rechts
* O:2 links, 4 rechts
* NA:1 aan de linkerkant, 1 rechts
2. Pas de coëfficiënten aan om de atomen in evenwicht te brengen:
* Zet een coëfficiënt van 2 voor C₁₇h₃₅coona aan de linkerkant:
cacl₂ (aq) + 2 c₁₇h₃₅coona (aq) → (c₁₇h₃₅coo) ₂ca (s) + NaCl (aq)
* Zet een coëfficiënt van 2 voor NaCl aan de rechterkant:
cacl₂ (aq) + 2 c₁₇h₃₅coona (aq) → (c₁₇h₃₅coo) ₂ca (s) + 2 NaCl (aq)
Nu is de vergelijking in evenwicht:
cacl₂ (aq) + 2 c₁₇h₃₅coona (aq) → (c₁₇h₃₅coo) ₂ca (s) + 2 NaCl (aq)
Verklaring:
* calciumchloride (cacl₂) is een oplosbare ionische verbinding.
* Natriumoleaat (C₁₇h₃₅coona) is het primaire onderdeel van zeep en is ook oplosbaar.
* calcium oleate ((c₁₇h₃₅coo) ₂ca) is een onoplosbaar zout dat een neerslag vormt, waardoor het bekende "zeeproep" wordt veroorzaakt wanneer zeep wordt gebruikt in hard water dat calciumionen bevat.
* natriumchloride (NaCl) is tafelzout en blijft opgelost.
 Zouden planten of dieren de eerste levensvormen op aarde zijn geweest?
Zouden planten of dieren de eerste levensvormen op aarde zijn geweest?  Wat er nodig is om te herstellen van droogte
Wat er nodig is om te herstellen van droogte Is een uitstekende Lyre Bird Carnivore of Herbivore?
Is een uitstekende Lyre Bird Carnivore of Herbivore?  Verboden industrieel oplosmiddel werpt nieuw licht op methaanmysterie (update)
Verboden industrieel oplosmiddel werpt nieuw licht op methaanmysterie (update) Rustige storing in Brits-Columbia die grote aardbevingen kan veroorzaken
Rustige storing in Brits-Columbia die grote aardbevingen kan veroorzaken
Hoofdlijnen
- Waar vinden sensorische neuronen en motor in?
- Hoe de vlieg zijn reproductieve mannetje selecteert
- Hoe werkt de wetenschap?
- Is er een verband tussen dankbaarheid en geluk?
- Wat zijn de producten en reactanten van cellulaire ademhaling waar komt het voor?
- Wat is wetenschappelijke naam?
- Wat zijn 4 natuurlijke bacteriemoordenaars?
- Wat zijn de functies van eiwitten in het lichaam?
- De evolutionaire voordelen van botgewicht onderzoeken
- Sneller en groener zuiveringsproces met kooldioxide

- Een snelle en nauwkeurige kijk op vezelversterkte composieten

- Kruiskoppelingsreacties:semiheterogene op PCN-Cu gebaseerde metallafotokatalyse
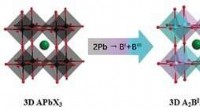
- Onderzoekers ontwikkelen halide dubbele perovskiet ferro-elektriciteit
- Onderzoekers ontwikkelen 3D-geprinte biomaterialen die op verzoek worden afgebroken

 Molecuul dicteert hoe stamcellen reizen
Molecuul dicteert hoe stamcellen reizen  Rechtbank beveelt Italiaanse regering om risico's voor mobiele telefoons bekend te maken
Rechtbank beveelt Italiaanse regering om risico's voor mobiele telefoons bekend te maken Welke edelgassen zijn rood?
Welke edelgassen zijn rood?  Welke stof heeft covalente bindingen a MgBr2 b LiCl c NaCl d CO2 welke is het?
Welke stof heeft covalente bindingen a MgBr2 b LiCl c NaCl d CO2 welke is het?  Waar heeft een slinger de minste hoeveelheid kinetische energie?
Waar heeft een slinger de minste hoeveelheid kinetische energie?  Welke energiebron is niet op?
Welke energiebron is niet op?  Diagnostisch hulpmiddel helpt ingenieurs bij het ontwerpen van betere wereldwijde infrastructuuroplossingen
Diagnostisch hulpmiddel helpt ingenieurs bij het ontwerpen van betere wereldwijde infrastructuuroplossingen Video:U gebruikt desinfectiemiddelen verkeerd. Dit is wat je echt moet doen
Video:U gebruikt desinfectiemiddelen verkeerd. Dit is wat je echt moet doen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

