
Wetenschap
Waarom bevindt het 11e elektron van het natriumatoom zich in het derde energieniveau?
Inzicht in elektronenconfiguratie
* Atomisch nummer: Natrium heeft een atoomnummer van 11, wat betekent dat het 11 protonen en 11 elektronen heeft.
* energieniveaus: Elektronen bezetten specifieke energieniveaus rond de kern. Deze niveaus worden aangeduid als 1, 2, 3, enzovoort, met hogere aantallen die een hogere energie aangeven.
* Subblevers: Elk energieniveau is onderverdeeld in subulels (s, p, d, f), die ook variërende energieniveaus binnen een bepaald niveau hebben.
Natrium's elektronenconfiguratie
1. Eerste energieniveau (n =1): Het kan maximaal 2 elektronen bevatten (in het 'S' Subblevel). Dus de eerste twee elektronen van Natrium vullen dit niveau.
2. Tweede energieniveau (n =2): Dit niveau heeft 's' en 'P' Subblevels. De 's' Subblevel bevat 2 elektronen en het 'P' Subblevel bevat 6 elektronen (voor een totaal van 8). Natriums volgende 8 elektronen vullen dit niveau.
3. Derde energieniveau (n =3): Het 11e elektron gaat in het subbloed van het derde energieniveau.
Waarom niet het tweede energieniveau?
Het tweede energieniveau kan maximaal 8 elektronen bevatten. Natrium heeft al 8 elektronen in het tweede niveau. Om het 11e elektron te huisvesten, is het volgende beschikbare energieniveau het derde.
Sleutelpunt: Elektronen vullen de energieniveaus en sub -evers in een specifieke volgorde, volgens het AUFBAU -principe. Dit principe stelt dat elektronen eerst de laagst beschikbare energieniveaus bezetten.
Hoofdlijnen
- Hoe verhoudt DNA-forensisch onderzoek zich tot biologie?
- Wat de eerste paar cellen die vormen omdat ze elk type cel kunnen worden?
- Wat was de bijdrage aan de celtheorie?
- Wat is oogenisis?
- Welke twee kenmerken geven aan dat een cel een dier is en geen plantencel?
- Wat regelt de activiteit van melanocyten?
- Snelle reactie van Fish op klimaatverandering
- Welke verandering zou je in dode organismen in de loop van de tijd verwachten?
- Hoe is de wetenschap aanwezig in een schoolcafetaria?
- Studie onthult geheim 18e-eeuws portret

- Lab-on-a-chip helpt bij het zoeken naar menselijk DNA op plaats delict

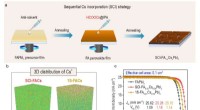
- Ontkoppeling van formamidinium–cesium perovskieten voor efficiënte fotovoltaïsche energie
- Onderzoekers doen inspanningen om parasitaire rondwormen te bestrijden
- Geïnspireerd door kombuchathee, ingenieurs creëren levende materialen

 Textiel dat zich ontwikkelt om aan de vraag naar duurzame materialen te voldoen
Textiel dat zich ontwikkelt om aan de vraag naar duurzame materialen te voldoen Wat is het beste materiaal om warmte uit lucht te absorberen?
Wat is het beste materiaal om warmte uit lucht te absorberen?  Wat is calcaan?
Wat is calcaan?  Hoe vormen anion van stikstofvormen?
Hoe vormen anion van stikstofvormen?  Wat is het elektrische potentieel op een punt in de ruimte als lading van 7,3 10-17 Coulombs met energie 6,4 joules heeft?
Wat is het elektrische potentieel op een punt in de ruimte als lading van 7,3 10-17 Coulombs met energie 6,4 joules heeft?  De reden dat de meeste extrasolaire planeten dicht bij hun oudersterren worden gevonden?
De reden dat de meeste extrasolaire planeten dicht bij hun oudersterren worden gevonden?  Welke elektromagnetische golven draagt de meeste energie?
Welke elektromagnetische golven draagt de meeste energie?  Wie was medeoprichter van de celtheorie?
Wie was medeoprichter van de celtheorie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


