
Wetenschap
Waarom leidt een ionische verbinding elektrische stroom wanneer deze wordt gesmolten?
1. De aard van ionische verbindingen
* Ionische verbindingen worden gevormd door de elektrostatische aantrekkingskracht tussen positief geladen ionen (kationen) en negatief geladen ionen (anionen). Deze ionen worden bij elkaar gehouden in een rigide, kristallijne roosterstructuur.
2. De vaste toestand:geen geleidbaarheid
* In de vaste toestand zijn de ionen op hun plaats op zijn plaats in het kristalrooster. Hoewel ze kosten hebben, kunnen ze niet vrij bewegen. Dit gebrek aan mobiele ladingsdragers is de reden waarom solide ionische verbindingen slechte elektriciteitsgeleiders zijn.
3. De vloeibare toestand:vrije ionen en geleidbaarheid
* Wanneer een ionische verbinding wordt gesmolten, worden de sterke elektrostatische krachten die de ionen bij elkaar houden verzwakt. De ionen krijgen de vrijheid om zich binnen de vloeistof te bewegen.
* Deze mobiliteit van ionen is cruciaal voor geleidbaarheid. Wanneer een spanning wordt toegepast over de gesmolten ionische verbinding, migreren de positief geladen ionen (kationen) naar de negatieve elektrode (kathode) en de negatief geladen ionen (anionen) migreren naar de positieve elektrode (anode).
* Deze beweging van geladen deeltjes vormt een elektrische stroom.
Samenvattend:
Het vermogen van gesmolten ionische verbindingen om elektriciteitsstengels uit de afgifte van ionen uit de rigide roosterstructuur te leiden, waardoor ze vrij kunnen bewegen en een elektrische stroom kunnen dragen.
 Cool-for-cash-gewas telen
Cool-for-cash-gewas telen Rijke landen lopen ver achter met klimaatbelofte van 100 miljard dollar:studie
Rijke landen lopen ver achter met klimaatbelofte van 100 miljard dollar:studie De rook van Canadese natuurbranden verstikt het Upper Midwest voor het tweede jaar op rij
De rook van Canadese natuurbranden verstikt het Upper Midwest voor het tweede jaar op rij  Studies tonen de impact aan van bosbeheer en ontbossing op het klimaat
Studies tonen de impact aan van bosbeheer en ontbossing op het klimaat  Het christendom verandert in Zuid-Afrika terwijl pinksterkerken en inheemse kerken groeien – wat zit er achter deze trend?
Het christendom verandert in Zuid-Afrika terwijl pinksterkerken en inheemse kerken groeien – wat zit er achter deze trend?
Hoofdlijnen
- Hoe kunnen uitstervingen de evolutie beïnvloeden van organismen die een gebeurtenis overleven?
- Ontdekken hoe een vleesetende schimmel wormen vangt en verteert
- Waarom is de Steenbokskeerkring belangrijk?
- Wat is sphlancologie?
- Team past nieuwe theorie toe om te leren hoe en waarom cellen differentiëren
- Hoe wordt de ontwikkeling van weefsels genoemd?
- Wordt Lily groeit uit een bol?
- Welk taxon heeft de meeste organismen?
- Ontdekking onthult hoe bacteriën schadelijke en nuttige virussen onderscheiden
- Onderzoekers pleiten voor beter gebruik van chemische hulpmiddelen om biomedisch onderzoek te verbeteren
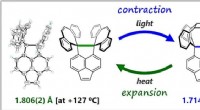
- Covalente koolstof-koolstofbindingen veel flexibeler dan verondersteld
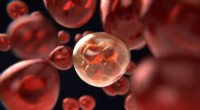
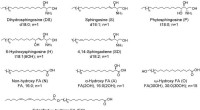
- Onderzoekers beschrijven het volledige scala aan ceramiden dat wordt aangetroffen in de bovenste laag van de menselijke huid
- Zonnebrandcrème en cosmetica kunnen koraal beschadigen door vetzuren te veranderen

- Grafeenkristallen groeien beter onder koperen afdekking

 Hoe trilt het medium in een dwarse golf met tweemaal kracht van energiekracht die onder rechtse hoeken wordt verstrekt om richting te reizen parallel de helft van de?
Hoe trilt het medium in een dwarse golf met tweemaal kracht van energiekracht die onder rechtse hoeken wordt verstrekt om richting te reizen parallel de helft van de?  Wat is er in het midden van de aarde naast de kern?
Wat is er in het midden van de aarde naast de kern?  Welke energieconversies die zich voordoen in verkeerslicht?
Welke energieconversies die zich voordoen in verkeerslicht?  Welke systemen in het lichaam zijn gerelateerd?
Welke systemen in het lichaam zijn gerelateerd?  Leven in de Melkweg:misschien is dit net zo goed als mogelijk?
Leven in de Melkweg:misschien is dit net zo goed als mogelijk?  Welk object reist 20 meter in 4 seconden wat is de snelheid van dit object?
Welk object reist 20 meter in 4 seconden wat is de snelheid van dit object?  Wat is planeet exacte baan- en rotatieperioden?
Wat is planeet exacte baan- en rotatieperioden?  Polytitaniumchloride pre-coagulatie voor vervuilingscontrole van keramisch membraan
Polytitaniumchloride pre-coagulatie voor vervuilingscontrole van keramisch membraan
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

