
Wetenschap
De chemische reactie weergegeven door 2 Nabr Plus Cl2 --2 NaCl BR2 is?
Dit is waarom:
* Enkele verplaatsing: In dit type reactie vervangt een meer reactief element een minder reactief element in een verbinding.
* De reactie: Chloor (CL₂) is reactiever dan broom (Br₂). Wanneer chloor reageert met natriumbromide (NABR), verplaatst het de broom, vormt natriumchloride (NaCl) en brengt broomgas vrij (Br₂).
Hier is een uitsplitsing van de reactie:
* reactanten:
* Natriumbromide (NABR)
* Chloorgas (CL₂)
* Producten:
* Natriumchloride (NaCl)
* Bromine Gas (Br₂)
De gebalanceerde chemische vergelijking:
2 NABR + CL₂ → 2 NaCl + Br₂
Sleutelpunten:
* De reactie treedt op omdat chloor reactiever is dan broom, wat betekent dat het een grotere neiging heeft om elektronen te krijgen.
* Dit type reactie wordt vaak gebruikt bij de productie van halogenen zoals broom.
 Waarom zou een pinniped in staat zijn om verder in water te reizen dan op het land?
Waarom zou een pinniped in staat zijn om verder in water te reizen dan op het land?  Australië moet zich inzetten voor een netto-nuluitstoot, zegt klimaatwetenschapper
Australië moet zich inzetten voor een netto-nuluitstoot, zegt klimaatwetenschapper Standpunt:Klimaatchaos beteugelen – waarom de natuur de onbezongen held is in onze zoektocht naar het netto nulpunt
Standpunt:Klimaatchaos beteugelen – waarom de natuur de onbezongen held is in onze zoektocht naar het netto nulpunt  High School Forensics Science Fair Projectideeën
High School Forensics Science Fair Projectideeën  Wat kunnen we leren van computationele archeologie?
Wat kunnen we leren van computationele archeologie?
Hoofdlijnen
- Voordelen en nadelen van XRD en XRF
- Hoe klonen werkt
- Hoe is jodium belangrijk voor levende organismen?
- Wat wordt als anarobisch metabolisme beschouwd?
- Wat eronder ligt:de groei van wortelcellen is opmerkelijk dynamisch, zo blijkt uit onderzoek
- Welk organisme vermenigvuldigt zich snel op basis van zijn wijze van aseksuele reproductie?
- Om de biosfeer voor toekomstige generaties te behouden, moeten mensen -?
- Wat zijn de 6 belangrijkste delen van een plant?
- Hoe vergelijken organen bij dieren en planten?
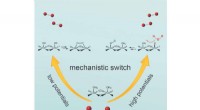
- Potentiaalafhankelijke schakelaar helpt bij het splitsen van water met behulp van kobaltoxidekatalysatoren
- Zoekmachine voor slim hout

- Wetenschappers elektrificeren aluminium om belangrijk proces te versnellen

- Wetenschappers ontwikkelen nieuwe theorie van moleculaire evolutie

- Onderzoek toont aan hoe de hechting tussen implantaten en bot kan worden verbeterd

 Welk type weer voor Nimbus -wolken?
Welk type weer voor Nimbus -wolken?  UnitedHealth en Amazon behoren tot de bieders voor Signify
UnitedHealth en Amazon behoren tot de bieders voor Signify Hoe een armillair gebied te bouwen
Hoe een armillair gebied te bouwen Waarom voer je transformatie uit van rustframe naar oneindig momentumframe?
Waarom voer je transformatie uit van rustframe naar oneindig momentumframe?  Te veel drankjes? Een nieuwe mobiele app kan je dat vertellen
Te veel drankjes? Een nieuwe mobiele app kan je dat vertellen  Is polijsten een fysieke verandering van metaal?
Is polijsten een fysieke verandering van metaal?  Hoe vind je de oorzaak van lichten die flikkeren wanneer een ander circuit wordt geactiveerd?
Hoe vind je de oorzaak van lichten die flikkeren wanneer een ander circuit wordt geactiveerd?  Hoe de ozonlaag
Hoe de ozonlaag
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

