
Wetenschap
Hoeveel schade kan 1 chlooratoom doen?
* chlooratomen zijn zeer reactief: Ze hebben een sterke neiging om te binden aan andere atomen om stabiele moleculen te vormen.
* chloor bestaat als een molecuul (CL2): Je zult geen enkele chlooratomen vinden die vrij rondzweven. Ze bestaan in paren als chloorgas (CL2).
* chloorgas kan schadelijk zijn: Chloorgas is een krachtig irriterend en kan ernstige schade aan het ademhalingssysteem veroorzaken als ze worden ingeademd.
Hier is hoe chloor schade kan veroorzaken:
* chloorgas (CL2): Het inademen van chloorgas kan de longen irriteren, wat hoesten, piepende ademhaling en zelfs de dood in extreme gevallen veroorzaken.
* chloorverbindingen: Wanneer chloor reageert met andere elementen, vormt het verbindingen zoals zoutzuur (HCL), een corrosief zuur dat in veel industriële processen wordt gebruikt.
* chloor in water: Chloor wordt toegevoegd aan drinkwater om schadelijke bacteriën te doden. Hoewel dit essentieel is, kunnen hoge niveaus van chloor in water huidirritatie, oogirritatie en zelfs gastro -intestinale problemen veroorzaken.
Samenvattend: Een enkel chlooratoom op zichzelf is onschadelijk, maar chloorgas en zijn verbindingen kunnen aanzienlijke gezondheidsrisico's vormen.
 NASA vindt Gabrielles kracht aan de noordkant
NASA vindt Gabrielles kracht aan de noordkant Europees parlement, EU-lidstaten bereiken doel om CO2 te verminderen
Europees parlement, EU-lidstaten bereiken doel om CO2 te verminderen Groene daken verbeteren de stedelijke omgeving – dus waarom hebben niet alle gebouwen ze?
Groene daken verbeteren de stedelijke omgeving – dus waarom hebben niet alle gebouwen ze?  Hawaii klaar om de verkoop van sommige zonnebrandmiddelen die koraal beschadigen te verbieden
Hawaii klaar om de verkoop van sommige zonnebrandmiddelen die koraal beschadigen te verbieden Hoe heet het als water land ontmoet?
Hoe heet het als water land ontmoet?
Hoofdlijnen
- Onderzoekers ontdekken een nieuwe familie bacteriën met een hoog farmaceutisch potentieel
- Waarom hebben tong veel bacteriën?
- Waartoe leidt hypothese?
- Wat zijn de twee hoofdcomponenten van een immuunrespons?
- Hoe evolueert het vermijden van inteelt bij planten?
- Wat produceren micro -organismen?
- Uit onderzoek blijkt dat alle Afrikaanse carnivoren risico lopen op verlies van hun bereik
- Wat is de naam van wetenschapper die dinosaurussen bestudeert?
- Welke twee kenmerken geven aan dat een cel een dier is en geen plantencel?
- Van broeikasgassen tot plastic:nieuwe katalysator voor recycling koolstofdioxide ontdekt

- Geleidende aard in kristalstructuren onthuld bij een vergroting van 10 miljoen keer

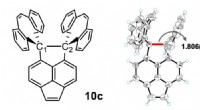
- Nieuw record voor lengte koolstof-koolstof enkelvoudige binding
- 2D-kristallen die voldoen aan 3D-curven veroorzaken spanning voor technische kwantumapparaten

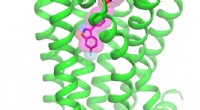
- Moleculaire geheimen onthuld:antipsychoticum gedokt in zijn receptor
 Hoe beïnvloedt een temperatuurdaling de druk van een ingesloten gas?
Hoe beïnvloedt een temperatuurdaling de druk van een ingesloten gas?  Een oververzadigde oplossing maken met suiker
Een oververzadigde oplossing maken met suiker  Wat is de ferretten -energie -rol in het ecosysteem?
Wat is de ferretten -energie -rol in het ecosysteem?  Kunststof elektronica met verflaag:polymeren uitlijnen voor hoge prestaties
Kunststof elektronica met verflaag:polymeren uitlijnen voor hoge prestaties Samenzweringstheoretici gaan actief op zoek naar hun online gemeenschappen
Samenzweringstheoretici gaan actief op zoek naar hun online gemeenschappen Wat is opwaartse kracht?
Wat is opwaartse kracht?  Kun je ijs laten gaan in een chemische verandering?
Kun je ijs laten gaan in een chemische verandering?  Hoe toon je voorbeelden van thermische energie?
Hoe toon je voorbeelden van thermische energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

