
Wetenschap
Wat is het Bohr-Rutherford-diagram voor fluor?
1. Bepaal het atoomnummer:
* Fluor (F) heeft een atoomnummer van 9. Dit betekent dat het 9 protonen en 9 elektronen heeft.
2. Teken de kern:
* Teken een grote cirkel in het midden om de kern weer te geven.
* Schrijf in de cirkel het aantal protonen, dat is 9.
3. Teken de elektronenschalen:
* eerste shell (k shell): Teken een kleinere cirkel rond de kern om de eerste elektronenschaal weer te geven. Plaats 2 stippen (die elektronen vertegenwoordigen) in deze cirkel.
* tweede shell (l shell): Teken nog een cirkel rond de eerste schaal. Plaats 7 stippen (die elektronen vertegenwoordigen) in deze cirkel.
Het voltooide diagram ziet er zo uit:
`` `
2
O --- o
7 o --- o 9
O --- o
O
`` `
Sleutelpunten:
* protonen: Gelegen in de kern, bepalen ze de identiteit van het element.
* neutronen: Ook in de kern dragen ze bij aan de massa van het atoom. Fluor heeft 10 neutronen, maar ze worden niet getoond in het Bohr-Rutherford-model.
* elektronen: Rond de kern in schelpen. De eerste schaal kan maximaal 2 elektronen bevatten en de tweede schaal kan maximaal 8 bevatten.
Laat het me weten als je de diagrammen voor andere elementen wilt zien!
 Aardbevingen in Oklahomas sterk verband met diepte van afvalwaterinjectie
Aardbevingen in Oklahomas sterk verband met diepte van afvalwaterinjectie Hoe maak je een tornado in een fles met afwasmiddel
Hoe maak je een tornado in een fles met afwasmiddel Onderzoeksduo vindt manier om verschuivingen in stroomgebieden te voorspellen als klimaatveranderingen
Onderzoeksduo vindt manier om verschuivingen in stroomgebieden te voorspellen als klimaatveranderingen Simulatie:stof had zich gelijkmatig over de aarde kunnen verspreiden na de inslag van de Chicxulub-asteroïde
Simulatie:stof had zich gelijkmatig over de aarde kunnen verspreiden na de inslag van de Chicxulub-asteroïde Wat is de betekenis van stengels?
Wat is de betekenis van stengels?
Hoofdlijnen
- Wat is de oorsprongsnaam uit Californië?
- Een cel besteedt ongeveer hoeveel van zijn cyclus in de M -fase?
- Wie is de vader van voedselmicrobiologie?
- Wat bestaat uit cellulose -micofibrillen?
- Wat is een wetenschappelijke eigenschap?
- Hoe worden gegevens gebruikt in de wetenschappelijke methode?
- Hoe verbeteren microscopen ons leven vandaag?
- Ontdekken hoe cellen gaten dichten (met video)
- Koraalgenoom onthult cysteïneverrassing
- AFRL bereikt schokkende doorbraak in materiaaltechnologie

- Onderzoekers vinden veelbelovende kandidaten voor nanodeeltjes voor het afvangen en omzetten van koolstofdioxide

- Een manier om polystyreen te recyclen tot waardevollere producten

- Bifunctionele ionomeren gebruiken als elektrolyten om ethyleen uit koolstofdioxide te synthetiseren
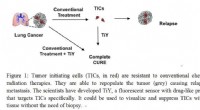
- Veelzijdige sensor tegen tumor-initiërende cellen
 Hoe is de luchtvochtigheid van invloed op het weer?
Hoe is de luchtvochtigheid van invloed op het weer?  Zonder eclipsbril naar een zonsverduistering kijken kan gevaarlijk zijn. Dit is wat u moet weten
Zonder eclipsbril naar een zonsverduistering kijken kan gevaarlijk zijn. Dit is wat u moet weten  Waarom zijn aardbevingen bergen en vulkanen in dezelfde classificatie?
Waarom zijn aardbevingen bergen en vulkanen in dezelfde classificatie?  Twinkelende pulsars observeren om mysterieus interstellair plasma te begrijpen
Twinkelende pulsars observeren om mysterieus interstellair plasma te begrijpen Wat is de interne temperatuur van een sterren?
Wat is de interne temperatuur van een sterren?  Een schokgeïnduceerd mechanisme voor het maken van organische moleculen
Een schokgeïnduceerd mechanisme voor het maken van organische moleculen Onderzoek lost de puzzel op waarom de hommel zo goed kan vliegen
Onderzoek lost de puzzel op waarom de hommel zo goed kan vliegen  Wat is de formulenaam voor aluminiumsulfaat?
Wat is de formulenaam voor aluminiumsulfaat?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

