
Wetenschap
Hoeveel mol waterstof zijn er nodig om 170000 g ammoniak te maken?
1. Schrijf de gebalanceerde chemische vergelijking:
N₂ (g) + 3H₂ (g) → 2nh₃ (g)
Deze vergelijking vertelt ons dat 3 mol waterstofgas (H₂) nodig is om te reageren met 1 mol stikstofgas (N₂) om 2 mol ammoniak (NH₃) te produceren.
2. Bereken de molaire massa ammoniak (NH₃):
* Stikstof (n) heeft een molaire massa van 14,01 g/mol
* Waterstof (H) heeft een molaire massa van 1,01 g/mol
* Molaire massa van NH₃ =14,01 g/mol + (3 * 1.01 g/mol) =17,04 g/mol
3. Converteer gram ammoniak naar mollen:
* Mol nH₃ =(170000 g nh₃) / (17,04 g / mol nh₃) =9976.53 mol nh₃
4. Gebruik de molverhouding van de gebalanceerde vergelijking om mol waterstof te vinden:
* Uit de vergelijking produceren 3 mol H₂ 2 mol NH₃.
* Mol h₂ =(9976.53 mol nh₃) * (3 mol H₂ / 2 mol nH₃) =14964.80 mol H₂
Daarom heeft u ongeveer 14964,80 mol waterstof nodig om 170000 g ammoniak te maken.
Hoofdlijnen
- Nieuwe methodieken om fraude te voorkomen bij het bepalen van de geografische herkomst van hazelnoten
- Insecten kunnen de voedselzelfvoorziening in Europa helpen vergroten, maar zullen ze aanslaan?
- Hoe verschillen vissen en vlinders van elkaar?
- Welk type axon verspreidt een actiepotentieel sneller?
- Wat hebben spam-e-mail en hiv met elkaar gemeen?
- Waarom is Hibiscus Flower een bedreigde plant?
- Bevat een voedselweb slechts één roofdier en ketting?
- Wat vormt een genenpool van bevolking?
- Hoe maak je een 3D-tandmodel voor een schoolproject
- Complexe objecten op cellulosebasis printen
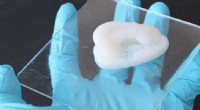
- Als toekomstige batterijen, hybride supercondensatoren zijn supergeladen

- Snelle en nauwkeurige meerkleurenbeeldvorming van biomoleculen nu mogelijk
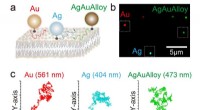
- N-C-bindingen rechtstreeks vanuit distikstof maken:samenvatting en perspectief

- Methaanverbruikende bacteriën kunnen de brandstof van de toekomst zijn
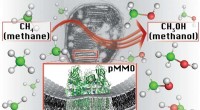
 Is een eclips gevaarlijker dan de zon?
Is een eclips gevaarlijker dan de zon?  NASA-satelliet vindt een wigvormige tropische storm Paulette
NASA-satelliet vindt een wigvormige tropische storm Paulette Wat zijn bloedstollingseiwitten?
Wat zijn bloedstollingseiwitten?  Welk type rots vormt zich als gevolg van het gewicht dat overliggende rotsen is?
Welk type rots vormt zich als gevolg van het gewicht dat overliggende rotsen is?  Sterrenmensen
Sterrenmensen  Wat is de edelgasconfiguratie van SN?
Wat is de edelgasconfiguratie van SN?  Hydrochloorzuur wordt toegevoegd aan vaste NaOH nadat de reactie volledige NaCl opgelost in water overblijft Wat zijn producten van deze chemische reactie?
Hydrochloorzuur wordt toegevoegd aan vaste NaOH nadat de reactie volledige NaCl opgelost in water overblijft Wat zijn producten van deze chemische reactie?  Hoe komeetstof de geschiedenis van het zonnestelsel onthult
Hoe komeetstof de geschiedenis van het zonnestelsel onthult
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


