
Wetenschap
Wat gebeurt er als natriumhydroxide reageert met koolstofdioxide?
Hier is de evenwichtige chemische vergelijking:
2 NaOH + CO2 → NA2CO3 + H2O
Hier is een uitsplitsing van wat er gebeurt:
* Stap 1: Koolstofdioxide lost op in water om koolzuur te vormen (H2CO3). Dit is een zwak zuur.
CO2 + H2O ⇌ H2CO3
* Stap 2: Het koolzuur reageert vervolgens met natriumhydroxide in een neutralisatiereactie.
H2CO3 + 2 NaOH → NA2CO3 + 2 H2O
Algemene reactie:
De algehele reactie combineert deze twee stappen om natriumcarbonaat en water te vormen:
2 NaOH + CO2 → NA2CO3 + H2O
Praktische toepassingen:
Deze reactie wordt gebruikt in verschillende toepassingen, waaronder:
* Koolstofdioxide schrobben: Natriumhydroxide wordt gebruikt om CO2 uit lucht of andere gasstromen te verwijderen. Dit is belangrijk in industriële processen, zoals in energiecentrales, waar CO2 -emissies een zorg zijn.
* Natriumcarbonaat maken: De reactie wordt gebruikt om natriumcarbonaat te produceren, een belangrijke industriële chemische stof die wordt gebruikt bij het maken van glas, wasmiddelen en andere producten.
Belangrijke opmerking:
* De reactie is exotherme, wat betekent dat het warmte vrijgeeft.
* Als de reactie in een gesloten container wordt uitgevoerd, kan de druk opgebouwd zijn als CO2 wordt verbruikt.
* De reactie wordt meestal uitgevoerd in waterige oplossing, waarbij natriumhydroxide in water wordt opgelost.
 Is de Olgas natuurlijk of gebouwd?
Is de Olgas natuurlijk of gebouwd?  Amerikaanse functionaris verklaart droogteplan klaar voor Colorado River
Amerikaanse functionaris verklaart droogteplan klaar voor Colorado River Harvey, Irma, Maria en Nate met pensioen door de Wereld Meteorologische Organisatie
Harvey, Irma, Maria en Nate met pensioen door de Wereld Meteorologische Organisatie Hoe heeft de wetenschap betrekking op de wetenschap?
Hoe heeft de wetenschap betrekking op de wetenschap?  Duizenden opzettelijk aangestoken branden duwen het regenwoud van Brazilië dicht bij het kantelpunt
Duizenden opzettelijk aangestoken branden duwen het regenwoud van Brazilië dicht bij het kantelpunt
Hoofdlijnen
- Onderzoekers tonen aan dat heparansulfaat de functies van groeifactoreiwitten aanpast
- Hoeveel cellen worden geschat in het volwassen menselijk lichaam?
- Wat betekent hypothese in de wetenschappelijke methode?
- Wat zijn de twee brede gebruiksgebieden en voorbeelden na een in kweek gekweekte gastheercel om klooncellen te vormen die gekloond genbelang bevatten?
- Wat betekent inoculeren in de microbiologie?
- Wat doet de conclusie in de wetenschappen?
- Waar staat T in cellen voor?
- Drukken genen zich uit via poëzie?
- Wat is een cochlea en wat zijn rol?
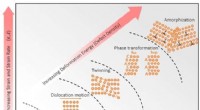
- Eilanden zonder structuur in metaallegeringen kunnen leiden tot hardere materialen
- Nieuwe reactie kan leiden tot een alternatieve benadering van ammoniakproductie

- Goedkope detector is als klittenband voor kankercellen
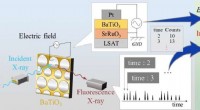
- Fijne structuur onthuld van potentieel alternatief voor loodverbinding gebruikt in sensoren
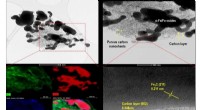
- Adsorberend materiaal ontwikkeld uit PET-flessen voor het verwijderen van antibiotica uit water
 Genereren van willekeurige getallen door fasefluctuaties te meten van een laserdiode met een silicon-on-in
Genereren van willekeurige getallen door fasefluctuaties te meten van een laserdiode met een silicon-on-in Grade School Robot Projects
Grade School Robot Projects Reageert natrium met andere elementen?
Reageert natrium met andere elementen?  Zijn goede warmtegeleiders ook elektriciteit?
Zijn goede warmtegeleiders ook elektriciteit?  Is een kwantum een kleine energie -eenheid?
Is een kwantum een kleine energie -eenheid?  Een bosgloed onthult ontwaken uit de winterslaap
Een bosgloed onthult ontwaken uit de winterslaap Wat bieden sterren?
Wat bieden sterren?  We begrijpen eindelijk hoe zuurstof reageert op platina
We begrijpen eindelijk hoe zuurstof reageert op platina
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

