
Wetenschap
Wat is de pH van ijzeroxide?
* pH is een maat voor de zuurgraad of alkaliteit van een oplossing. IJzeroxide is een vaste stof, geen oplossing.
* De pH van een oplossing die ijzeroxide bevat, hangt af van verschillende factoren:
* De vorm van ijzeroxide: Verschillende vormen (zoals hematiet, goethiet, magnetiet) kunnen verschillende effecten hebben op de pH.
* De aanwezigheid van andere stoffen: De pH van de oplossing kan worden beïnvloed door andere aanwezige chemicaliën of mineralen.
* De oplosbaarheid van het ijzeroxide: De hoeveelheid ijzeroxide die oplost in de oplossing beïnvloedt de pH.
Hier is een meer genuanceerde uitleg:
* Wanneer ijzeroxide in contact komt met water, kan het hydrolyse ondergaan reacties. Dit betekent dat watermoleculen interageren met het ijzeroxide en ionen in de oplossing vrijgeven.
* Afhankelijk van de specifieke omstandigheden kunnen deze ionen de oplossing enigszins zuur of basic maken. Als de oplossing bijvoorbeeld zuur wordt, heeft deze een pH lager dan 7. Als de oplossing eenvoudig wordt, heeft deze een pH boven 7.
Samenvattend:
* IJzeroxide zelf heeft geen specifieke pH.
* De pH van een oplossing die ijzeroxide bevat, hangt af van de specifieke vorm van ijzeroxide, de aanwezigheid van andere stoffen en de oplosbaarheid ervan.
 Hoe beschermen Beluga's zichzelf?
Hoe beschermen Beluga's zichzelf?  De productie van biobrandstof uit algen is noch ecologisch, noch commercieel duurzaam
De productie van biobrandstof uit algen is noch ecologisch, noch commercieel duurzaam Bloemen en planten gevonden in gematigde bossen
Bloemen en planten gevonden in gematigde bossen Huisontwikkelaars kunnen het geheime wapen zijn om de luchtkwaliteit te verbeteren
Huisontwikkelaars kunnen het geheime wapen zijn om de luchtkwaliteit te verbeteren Definitie van een Seizoensgebonden Hoogwatertafel
Definitie van een Seizoensgebonden Hoogwatertafel
Hoofdlijnen
- Wat is maïsplastic?
- Hoe vissen evolueerden om te lopen
- Koningin of arbeider? Flexibiliteit tussen rollen is afhankelijk van slechts een paar genen
- Welke lipiden vind je geassocieerd met de celmembranen en organellen van cellen?
- Wat zijn de vijf verschillende bewijslijnen voor evolutie?
- Hoe reproduceren pindaplanten zich?
- Hoe een organisme eruit ziet, ongeacht de allelen van het type wordt gerefereerd als wat?
- Algemene kenmerken van Protista
- Welk type cel is een rozennel?
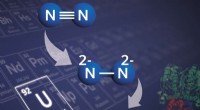
- Een op uranium gebaseerde verbinding verbetert de productie van stikstofproducten
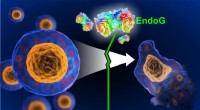
- Biochemici ontdekken een enzym om celdood te stoppen
- Het begin van een revolutie in verpakkingen

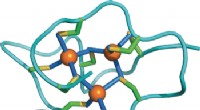
- Zwaar metaalbindend domein in een cysteïnerijk eiwit kan de aanpassing van de zeeslak aan metaalstress zijn
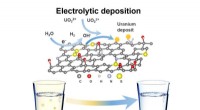
- Grafeenschuim gebruiken om gifstoffen uit drinkwater te filteren
 Is de sleutel en geleider van elektriciteit?
Is de sleutel en geleider van elektriciteit?  Heeft vroegtijdig stemmen invloed op politieke campagnes en verkiezingsresultaten?
Heeft vroegtijdig stemmen invloed op politieke campagnes en verkiezingsresultaten?  Kun je uitleggen waarom de maan geen lichtbron is?
Kun je uitleggen waarom de maan geen lichtbron is?  Waarom wordt de eenheid van het bedrag hetzelfde gedaan als voor energie?
Waarom wordt de eenheid van het bedrag hetzelfde gedaan als voor energie?  MO-SCI gaat SRNL's unieke poreus ommuurde holle glazen microsferen vervaardigen
MO-SCI gaat SRNL's unieke poreus ommuurde holle glazen microsferen vervaardigen Wetenschappers brengen polymeren in focus op atomaire schaal
Wetenschappers brengen polymeren in focus op atomaire schaal Onderzoekers ontwikkelen semi-vloeibare metaalanode voor batterijen van de volgende generatie
Onderzoekers ontwikkelen semi-vloeibare metaalanode voor batterijen van de volgende generatie Nieuwe tool voorspelt risico op plantenziekten en plagen wereldwijd
Nieuwe tool voorspelt risico op plantenziekten en plagen wereldwijd
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

