
Wetenschap
Welke metalloïden zouden chemische eigenschappen hebben die vergelijkbaar zijn met broom?
Dit is waarom:
* elektronegativiteit: Halogenen zijn zeer elektronegatief, wat betekent dat ze elektronen sterk aantrekken. Metalloïden hebben over het algemeen een lagere elektronegativiteit dan halogenen.
* Oxidatie stelt: Halogenen hebben meestal negatieve oxidatietoestanden en krijgen elektronen om anionen te vormen. Metalloïden kunnen zowel positieve als negatieve oxidatietoestanden vertonen, afhankelijk van het specifieke element en de bindingsomgeving.
* Reactiviteit: Halogenen zijn zeer reactieve en vormen gemakkelijk verbindingen met andere elementen. Metalloïden kunnen reactief zijn, maar hun reactiviteit is vaak minder uitgesproken en afhankelijker van specifieke omstandigheden.
Daarom zijn er geen metalloïden met chemische eigenschappen vergelijkbaar met broom . Terwijl sommige metalloïden zoals selenium en tellurium Deel enkele overeenkomsten met halogenen in termen van hun locatie op het periodieke tabel en hun vermogen om anionen te vormen, hun algehele chemische gedrag is heel anders.
 Hoe onderzoekers water uit de lucht oogsten
Hoe onderzoekers water uit de lucht oogsten  Is de claim van Australië op Antarctica in gevaar?
Is de claim van Australië op Antarctica in gevaar?  Wilt u uw gezondheid verbeteren? Ga naar een nationaal park en absorbeer de geluiden
Wilt u uw gezondheid verbeteren? Ga naar een nationaal park en absorbeer de geluiden  De strijd om het leven in de Dode Zee-sedimenten:necrofagie als overlevingsmechanisme
De strijd om het leven in de Dode Zee-sedimenten:necrofagie als overlevingsmechanisme De zuurstofrevolutie veranderde het milieu dramatisch Welke aanpassingen maakten gebruik van de aanwezigheid vrij in oceanen en atmosfeer?
De zuurstofrevolutie veranderde het milieu dramatisch Welke aanpassingen maakten gebruik van de aanwezigheid vrij in oceanen en atmosfeer?
Hoofdlijnen
- Wat is Evolution Deceit?
- Wat speelt een actieve rol in eiwitsynthese?
- Welke rol speelt een kikker in het ecosysteem?
- Wat is verspreiding in de wetenschap?
- Waarom hebben eencellige organismen geen complexe structuren nodig voor gasuitwisseling?
- Onderzoekers tonen aan dat geïntroduceerde tardigrade-eiwitten de stofwisseling in menselijke cellen kunnen vertragen
- Onderzoekers suggereren dat mechanische druk een belangrijke gebeurtenis in de HIV-infectie veroorzaakt
- Hoe schat ik de celgrootte met behulp van een microscoop?
- Het ontrafelen van de redenen waarom massale uitstervingen plaatsvinden
- Onderzoekers synthetiseren nieuwe vloeibare kristallen die gerichte transmissie van elektriciteit mogelijk maken

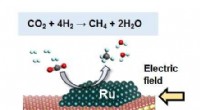
- Nieuwe methode zet koolstofdioxide om in methaan bij lage temperaturen
- Nanodiamanten als fotokatalysatoren

- Licht kan worden gebruikt om de genfunctie te regelen

- Onderzoekers vinden nieuwe vorm voor hydrofobe moleculen in water

 Welke dieren zijn circadiane ritmes?
Welke dieren zijn circadiane ritmes?  Wat is meer kans om een ionische binding te vormen een silicium en zuurstof B C koolstofwaterstof D magnesiumzuurstof?
Wat is meer kans om een ionische binding te vormen een silicium en zuurstof B C koolstofwaterstof D magnesiumzuurstof?  Het vernietigen van de rivierbossen van Nigeria is slecht voor het zoetwaterecosysteem
Het vernietigen van de rivierbossen van Nigeria is slecht voor het zoetwaterecosysteem Goedkoop navigatiesysteem voor onbemande antennesystemen
Goedkoop navigatiesysteem voor onbemande antennesystemen Reisgigant Expedia zegt dat het er 3 gaat schrappen 000 banen
Reisgigant Expedia zegt dat het er 3 gaat schrappen 000 banen Een pseudo-magnetisch veld met een groot oppervlak in grafeen afstemmen op een kristal met verschillende symmetrie
Een pseudo-magnetisch veld met een groot oppervlak in grafeen afstemmen op een kristal met verschillende symmetrie Wat is een bolvormig molecuul?
Wat is een bolvormig molecuul?  Vortexringen kunnen de celafgifte helpen, celvrije eiwitproductie
Vortexringen kunnen de celafgifte helpen, celvrije eiwitproductie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

