
Wetenschap
Wat is de empirische formule voor ijzerchloride als deze 55,85 gram en 106,5 chloor bevat?
Hier leest u hoe u de empirische formule voor ijzerchloride kunt bepalen:
1. Converteer grams naar mollen
* ijzer (Fe): 55,85 g Fe / 55.845 g / mol Fe =1.000 mol Fe
* chloor (CL): 106,5 g CL / 35,45 g / mol CL =3.000 mol CL
2. Vind de molverhouding
* Verdeel het aantal mol van elk element door het kleinste aantal mol (dat in dit geval 1.000 mol is):
* Fe:1.000 mol / 1.000 mol =1
* CL:3.000 mol / 1.000 mol =3
3. Schrijf de empirische formule
* De molverhouding vertelt ons dat de empirische formule fecl₃ is .
Daarom is de empirische formule voor ijzerchloride met deze verhoudingen Fecl₃.
 Wat geldt voor de meeste organische verbindingen?
Wat geldt voor de meeste organische verbindingen?  Polaron-grensvlakentropie als route naar hoge thermo-elektrische prestaties in DAE-gedoteerde PEDOT:PSS-films
Polaron-grensvlakentropie als route naar hoge thermo-elektrische prestaties in DAE-gedoteerde PEDOT:PSS-films  Wat zijn de alternatieve opgeloste zuurstofcavengers anders dan hydrazine voor HP -ketelvoedingswater?
Wat zijn de alternatieve opgeloste zuurstofcavengers anders dan hydrazine voor HP -ketelvoedingswater?  Wat is het kleinste aantal onderdelen in een compound?
Wat is het kleinste aantal onderdelen in een compound?  Welke van de volgende vertegenwoordigt een moleculaire verbinding xe zno SO2 BEF2?
Welke van de volgende vertegenwoordigt een moleculaire verbinding xe zno SO2 BEF2?
 Zou een diep-aardse watercyclus ons begrip van planetaire evolutie veranderen?
Zou een diep-aardse watercyclus ons begrip van planetaire evolutie veranderen? Afbeelding:Proba-V-afbeeldingen Salar de Uyuni
Afbeelding:Proba-V-afbeeldingen Salar de Uyuni Waar bestaat de aarde meestal uit?
Waar bestaat de aarde meestal uit?  Ontbossing verduistert de zeeën boven het op een na grootste rif ter wereld
Ontbossing verduistert de zeeën boven het op een na grootste rif ter wereld Hoe psychologie mensen kan helpen een klimaatvriendelijker leven te leiden – lessen van over de hele wereld
Hoe psychologie mensen kan helpen een klimaatvriendelijker leven te leiden – lessen van over de hele wereld
Hoofdlijnen
- Wat is de belangrijkste erkenning van codominantie?
- Zijn de dochtercellen identiek of genetisch verschillend?
- Welke soort lijkt het meest op mensen?
- Waarom hebben de bevolking variaties in bepaalde eigenschappen?
- Hoeveel organismen moeten er in een voedselketen zijn om cellulaire ademhaling uit te voeren?
- Is suiker zuur of onoplosbaar in water?
- Waarom heeft de mens cultuur?
- Wanneer sporen ontkiemen, welke generatie ontwikkelt zich?
- Wat is een plant die bestaat uit zowel schimmels als algen?
- Wetenschappers programmeren eiwitten om precies te paren
- Wetenschappers ontwikkelen antibacterieel gelverband met durian husk

- Afbreekbare op suiker gebaseerde polymeren kunnen nuttige moleculaire vracht opslaan en vrijgeven

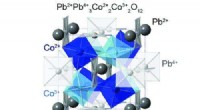
- Gemengde valentietoestanden in loodperovskieten
- Rekbare en knijpende zachte sensoren een stap dichterbij dankzij nieuwe hechtmethode
 Hoe verhoudt de kleur van sterren zich tot massa?
Hoe verhoudt de kleur van sterren zich tot massa?  Hoe Linearity
Hoe Linearity Aardgebonden instrument analyseert licht van planeten rond verre sterren
Aardgebonden instrument analyseert licht van planeten rond verre sterren Wat is energiebron voor kinesthetisch?
Wat is energiebron voor kinesthetisch?  In de pijplijn:een oplossing voor een 130 jaar oud probleem
In de pijplijn:een oplossing voor een 130 jaar oud probleem Leiden stadstuinen tot gentrificatie? Niet in Detroit, zo blijkt uit onderzoek
Leiden stadstuinen tot gentrificatie? Niet in Detroit, zo blijkt uit onderzoek  0-D:nuldimensionale kwantumstippen geïdentificeerd door onderzoekers
0-D:nuldimensionale kwantumstippen geïdentificeerd door onderzoekers Wat is de definitie van stationaire elektriciteit?
Wat is de definitie van stationaire elektriciteit?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

