
Wetenschap
Wat is de relatie tussen waterstofbinding en cohesie?
* waterstofbinding: Waterstofbindingen zijn relatief zwakke attracties tussen een waterstofatoom covalent gekoppeld aan een sterk elektronegatief atoom (zoals zuurstof in water) en een elektronpaar in het aangrenzende molecuul. Dit creëert een "plakkerige" interactie tussen watermoleculen.
* cohesie: Cohesie verwijst naar de aantrekkingskracht tussen moleculen van dezelfde stof. In water leiden de sterke waterstofbindingen tussen watermoleculen tot een hoge mate van cohesie. Dit betekent dat watermoleculen "samen" plakken ".
Hier is hoe deze relatie zich afspeelt:
* Hoge oppervlaktespanning: De sterke cohesie van watermoleculen creëert een hoge oppervlaktespanning. Dit is de reden waarom water druppeltjes vormt en waarom insecten op water kunnen lopen.
* Capillaire actie: Cohesie draagt ook bij aan capillaire actie. Watermoleculen worden tot elkaar aangetrokken en tot de wanden van smalle buizen, waardoor water tegen de zwaartekracht in buizen of poreuze materialen stijgt.
* Oplosbaarheid van polaire moleculen: De polariteit van watermoleculen, als gevolg van waterstofbinding, maakt het mogelijk andere polaire moleculen op te lossen. De aantrekkingskracht tussen watermoleculen en polaire moleculen zoals suikers en zouten is cruciaal voor veel biologische processen.
Samenvattend: Waterstofbindingen tussen watermoleculen creëren een sterke cohesie, wat leidt tot verschillende belangrijke eigenschappen van water, waaronder hoge oppervlaktespanning, capillaire werking en het vermogen om polaire moleculen op te lossen.
 Wat zijn de 4 belangrijkste punten van natuurlijke selectie?
Wat zijn de 4 belangrijkste punten van natuurlijke selectie?  Klimaatverandering maakt zomerweer stormachtiger en toch meer stagnerend
Klimaatverandering maakt zomerweer stormachtiger en toch meer stagnerend Klimaatverandering vertraagt de Atlantische stromingen die Europa en de Atlantische kust verwarmen
Klimaatverandering vertraagt de Atlantische stromingen die Europa en de Atlantische kust verwarmen Mobiele telefoon-app levert nauwkeurige regenvalinformatie aan het publiek
Mobiele telefoon-app levert nauwkeurige regenvalinformatie aan het publiek Nieuwe webtool zal militaire, samenwerking tussen windenergie-industrie
Nieuwe webtool zal militaire, samenwerking tussen windenergie-industrie
Hoofdlijnen
- Anadrome vissen gaan de ene manier catadromous doen het de andere diadromous beide kanten op wat?
- Welke objecten zijn te vinden in de exosophere?
- Wat hebben alle levende organismen gemeen?
- Wat betekent dat gegevens verkregen?
- Hoe organiseren wetenschappers?
- Wat is de oorsprong van het woordfenomeen?
- Wat is evolutiedefinitie?
- Wat doen alle cellen?
- Wanneer moet u uw hond castreren of steriliseren? Onderzoekers actualiseren richtlijnen
- Een unieke katalysator maakt de weg vrij voor plastic upcycling
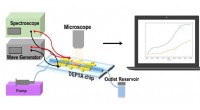
- Onderzoekers ontwikkelen lab-on-a-chip voor gepersonaliseerde monitoring van de werkzaamheid van geneesmiddelen
- Kleine implantaten voor cellen zijn functioneel in vivo
- Een nieuw magnetisch materiaal en opnameproces om de datacapaciteit enorm te vergroten

- Tikken geheimen van Aussie spiders unieke zijde

 Van groeiende wortels tot aanwijzingen over hoe stamcellen hun lot bepalen
Van groeiende wortels tot aanwijzingen over hoe stamcellen hun lot bepalen  Studie vergelijkt drie top-atoomklokken met recordnauwkeurigheid over zowel glasvezel als lucht
Studie vergelijkt drie top-atoomklokken met recordnauwkeurigheid over zowel glasvezel als lucht Wanneer waargenomen in een traagheidskader van referentie alle objecten die geen krachten ervaren zullen lijken?
Wanneer waargenomen in een traagheidskader van referentie alle objecten die geen krachten ervaren zullen lijken?  Wat is het momentum van een auto van 750 kg die reist met snelheid 25 ms?
Wat is het momentum van een auto van 750 kg die reist met snelheid 25 ms?  Fusie tussen twee sterren leidde tot blauwe superreus, iconische supernova
Fusie tussen twee sterren leidde tot blauwe superreus, iconische supernova Hoe schrijf je zinkchloride als chemische formule?
Hoe schrijf je zinkchloride als chemische formule?  Is het een vogel of een dinosaurus? Fossielen uit het Teylers Museum in Nederland bezoeken in het geheim de Britse synchrotron
Is het een vogel of een dinosaurus? Fossielen uit het Teylers Museum in Nederland bezoeken in het geheim de Britse synchrotron  Wat is de structuur die kern omsluit?
Wat is de structuur die kern omsluit?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

