
Wetenschap
Hoe lichter de atoom minder massa in één mol van dat atoom?
* Atomische massa: De massa van een atoom wordt voornamelijk bepaald door het aantal protonen en neutronen in zijn kern. Lichte atomen hebben minder protonen en neutronen.
* mol: Een mol is een specifiek aantal deeltjes (6.022 x 10^23). Eén mol van elk element bevat hetzelfde aantal atomen.
* massa van één mol: Omdat een mol van elk element hetzelfde aantal atomen bevat, is de massa van één mol recht evenredig met de atomaire massa van het element. Daarom zullen lichtere atomen met lagere atoommassa's een lagere massa per mol hebben.
Voorbeeld:
* Waterstof (H) heeft een atoommassa van ongeveer 1 atomaire massa -eenheid (AMU).
* Zuurstof (O) heeft een atoommassa van ongeveer 16 AMU.
Dit betekent dat één mol waterstof een massa van ongeveer 1 gram zal hebben, terwijl één mol zuurstof een massa van ongeveer 16 gram zal hebben.
 Kleine plankton-aandrijfprocessen in de oceaan die twee keer zoveel koolstof vastleggen als wetenschappers dachten
Kleine plankton-aandrijfprocessen in de oceaan die twee keer zoveel koolstof vastleggen als wetenschappers dachten Wetenschappers volgen gigantische oceaanvortex vanuit de ruimte
Wetenschappers volgen gigantische oceaanvortex vanuit de ruimte Afbeelding:branden in Californië en Oregon nog steeds laaiend
Afbeelding:branden in Californië en Oregon nog steeds laaiend De wildernis van een baai van Lake Ontario laat zien hoe kusthabitats lijden onder het veranderende klimaat, menselijke keuzes
De wildernis van een baai van Lake Ontario laat zien hoe kusthabitats lijden onder het veranderende klimaat, menselijke keuzes Wat doen de bladeren van een plant?
Wat doen de bladeren van een plant?
Hoofdlijnen
- Wat zijn wetenschappelijke namen voor 3 soorten bloedcellen?
- Wat zijn strikte aerobes?
- Hoe gebruiken wetenschappers wetenschappelijke notatie?
- Wat zijn 25 organismen waaruit een Web in Oceanic Food bestaat?
- Waarom fungeert eten niet als antigeen?
- Wat zijn de RNA -stikstofbases?
- Welk vaccin wordt geproduceerd door slechts een deel van het virale genoom te gebruiken?
- Slapende honden laten liggen? Nieuw onderzoek suggereert dat ze zelfs tijdens het snoozen vocalisaties kunnen verwerken
- Wat is het doel van mitose?
- Nobelprijs voor scheikunde eert groenere manier om moleculen te bouwen

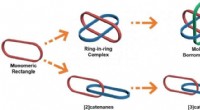
- Alles-in-één strategie voor metalla[3]catenanen, Borromeïsche ringen en ring-in-ring-complex
- Video:Werken anti-rimpelcrèmes?

- Naar een stamcelmodel van de ontwikkeling van het menselijk zenuwstelsel
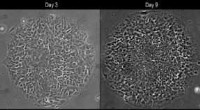
- Een stap dichter bij ontwerp-on-demand steigers voor weefselregeneratie

 Hoe interageert de door de stad veroorzaakte opwarming in Beijing met de luchttemperatuur in de zomer?
Hoe interageert de door de stad veroorzaakte opwarming in Beijing met de luchttemperatuur in de zomer? AAA test hits versus missers in AEB-systemen
AAA test hits versus missers in AEB-systemen Geavanceerde experimentele opzet breidt de jacht op verborgen donkere materiedeeltjes uit
Geavanceerde experimentele opzet breidt de jacht op verborgen donkere materiedeeltjes uit  Energie opgeslagen in rotsen als een veranderingsvorm?
Energie opgeslagen in rotsen als een veranderingsvorm?  Hoe vind je hoeveel kilogram 16 pond is?
Hoe vind je hoeveel kilogram 16 pond is?  Wetenschappers ontwarren nanobuisjes om hun potentieel in de elektronica-industrie vrij te maken (met video)
Wetenschappers ontwarren nanobuisjes om hun potentieel in de elektronica-industrie vrij te maken (met video) Hoe een afstandsbediening auto te bouwen voor een Science Fair Project
Hoe een afstandsbediening auto te bouwen voor een Science Fair Project  Wat is het punt in het interieur waar de energie van een aardbeving vrijgegeven?
Wat is het punt in het interieur waar de energie van een aardbeving vrijgegeven?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

