
Wetenschap
Hoeveel S -atomen zijn aanwezig in 7,00 mg allicine?
1. Begrijp de formule:
* Allicine heeft de chemische formule c₆h₁₀os₂. Dit vertelt ons dat er twee zwavel (s) atomen zijn in elk molecuul allicine.
2. Converteer milligram naar gram:
* 7,00 mg =0,00700 g
3. Bereken de molaire massa van allicine:
* C:6 atomen * 12.01 g/mol =72,06 g/mol
* H:10 atomen * 1,01 g/mol =10,10 g/mol
* O:1 atoom * 16.00 g/mol =16,00 g/mol
* S:2 atomen * 32.07 g/mol =64,14 g/mol
* Totale molaire massa van allicine =162,30 g/mol
4. Bereken de mol allicine:
* mol =massa / molaire massa
* mol =0,00700 g / 162.30 g / mol =4,31 x 10⁻⁵ mol
5. Bereken het aantal S -atomen:
* We weten dat er 2 s atomen per molecuul allicine zijn.
* Gebruik het nummer van Avogadro (6.022 x 10²³ Moleculen/mol) om mol om te zetten in moleculen.
* Vermenigvuldig vervolgens met het aantal S -atomen per molecuul.
* Aantal S -atomen =(4.31 x 10⁻⁵ mol allicine) * (6.022 x 10²³ Moleculen/mol) * (2 s atomen/molecuul)
* Aantal S -atomen ≈ 5.19 x 10¹⁹ S Atoms
Daarom zijn ongeveer 5,19 x 10¹⁹ s atomen aanwezig in 7,00 mg allicine.
 Toenemende klimaatvariabiliteit zal de armste landen ter wereld treffen
Toenemende klimaatvariabiliteit zal de armste landen ter wereld treffen NASA ziet ex-tropische cycloon Gita Nieuw-Zeeland treffen
NASA ziet ex-tropische cycloon Gita Nieuw-Zeeland treffen Met dik ijs verdwenen, Arctisch zee-ijs verandert langzamer
Met dik ijs verdwenen, Arctisch zee-ijs verandert langzamer AI-model toont belofte om sneller te genereren, nauwkeurigere weersvoorspellingen
AI-model toont belofte om sneller te genereren, nauwkeurigere weersvoorspellingen Amazone-mangrovebos slaat twee keer zoveel koolstof op per hectare als beroemd regenwoud in de regio
Amazone-mangrovebos slaat twee keer zoveel koolstof op per hectare als beroemd regenwoud in de regio
Hoofdlijnen
- Hoe zou een dieren zijn extra opgeslagen suiker vrijgeven?
- Sperma zijn, of niet sperma? Ontdekking van een genetische schakelaar die het lot van kiemcellen bepaalt
- Hoe vissen tegelijkertijd geluiden horen en maken
- Wat zijn de DNA -moleculen gevonden in celorganel?
- Ontdekkingen van donkere materie kunnen licht werpen op nieuwe behandelingen voor ziekten
- Welke cel heeft een gebrek aan membraangebonden kern?
- Waar resulteren gistglucose en water in?
- In wezen ruw endoplasmatisch reticulum en belangrijk metabolisch in zenuwcellen?
- Hoe de toekomst van de Amerikaanse maïs-, soja- en tarweproductie afhangt van duurzaam grondwatergebruik
- Gebruik van zonlicht om de toekomst te voeden via covalente organische raamwerken

- Afvangen en omzetten van kooldioxide in een bruikbaar product

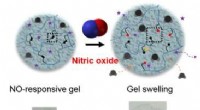
- Wetenschappers ontwikkelen potentieel therapeutische gel, die stikstofmonoxide detecteert, absorbeert overtollig vocht en geeft medicijnen af
- Een veiligere manier voor de politie om drugsbewijs te testen

- Chemici leren computerprogramma's om krachten tussen atomen nauwkeurig te modelleren

 Golfenergieomzetters zijn niet gericht op de toename van energie in de afgelopen eeuw
Golfenergieomzetters zijn niet gericht op de toename van energie in de afgelopen eeuw Wanneer een object centripetale versnelling ervaart, in welke richting versnelt het dan?
Wanneer een object centripetale versnelling ervaart, in welke richting versnelt het dan?  De overgang naar een koolstofarme economie moet inclusief zijn, zeggen onderzoekers
De overgang naar een koolstofarme economie moet inclusief zijn, zeggen onderzoekers Kwantumcomputers draaien het script om over spinchemie
Kwantumcomputers draaien het script om over spinchemie Een mineraal met zijdeachtige glans die wordt gebruikt in babypoeder?
Een mineraal met zijdeachtige glans die wordt gebruikt in babypoeder?  Gate Valve Vs. Kogelkraan
Gate Valve Vs. Kogelkraan  Hoe helpt marihuana de gezondheid van mensen
Hoe helpt marihuana de gezondheid van mensen  'S Werelds eerste systeem voorspelt opwarming van meren wereldwijd
'S Werelds eerste systeem voorspelt opwarming van meren wereldwijd
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

