
Wetenschap
Als u de volgende woordvergelijking herschrijft als een gebalanceerde chemische stof, wat zal de coëfficiënt en symbool voor fluor stikstof trifluoride zijn - plus fluor?
1. Identificeer de reactanten en producten:
* reactanten: Stikstof trifluoride (NF₃) en fluor (f₂)
* Product: We moeten uitzoeken welke vormen wanneer deze reageren. Stikstof trifluoride is een stabiele verbinding, dus de fluor zal er waarschijnlijk aan toevoegen.
2. Schrijf de onevenwichtige vergelijking:
NF₃ + F₂ →?
3. Bepaal het product:
Fluor zal waarschijnlijk bijdragen aan het stikstof trifluoride, waardoor een hoger fluoride van stikstof wordt gevormd. Het meest waarschijnlijke product is stikstof pentafluoride (NF₅).
4. Schrijf de volledige ongebalanceerde vergelijking:
NF₃ + F₂ → NF₅
5. Breng de vergelijking in evenwicht:
* stikstof (n): Er is één n aan elke kant, dus deze is in balans.
* fluor (f): Er zijn 3 F aan de linkerkant en 5 F rechts. Om in evenwicht te zijn, hebben we 2 nf₃ moleculen en 1 F₂ molecuul nodig:
2nf₃ + f₂ → 2nf₅
6. Bepaal de coëfficiënt en het symbool voor fluor:
* Coëfficiënt: De fluorcoëfficiënt (f₂) is 1
* Symbool: Het symbool voor fluor is f
Daarom is de gebalanceerde chemische vergelijking:
2nf₃ + f₂ → 2nf₅
 Wetenschapsexperimenten met planten voor kinderen
Wetenschapsexperimenten met planten voor kinderen Branden in Australië duiken op op reeds afgebrande plaatsen
Branden in Australië duiken op op reeds afgebrande plaatsen Socioloog vraagt wat het betekent om Amerikaan te zijn
Socioloog vraagt wat het betekent om Amerikaan te zijn  Wat betekent luchtweergave in de wetenschap?
Wat betekent luchtweergave in de wetenschap?  Onderzoekers ontwikkelen nieuwe kaarten om cruciale Arctische ecosystemen te helpen beschermen
Onderzoekers ontwikkelen nieuwe kaarten om cruciale Arctische ecosystemen te helpen beschermen
Hoofdlijnen
- Wat is een cel die geen kern heeft?
- Wat is de oorsprong van Sinterklaas?
- Wat is het enzym dat de dubbele helix uit elkaar breekt en twee sjabloonstrengen blootstelt?
- Welke organel moet aanwezig zijn in grote aantallen in spiercellen?
- Wat is het verschil tussen zoölogie en sociologie?
- Wat vormen de tapijten van DNA -molecuul?
- Hoe orang -oetans zich voortplanten?
- Nieuwe Japanse leliesoort geïdentificeerd, eerste toevoeging aan de sukashiyuri-groep in 110 jaar
- Waar strijden organismen volgens de evolutietheorie van Darwin om?
- Detectie van ethyleen, het fruitrijpingshormoon

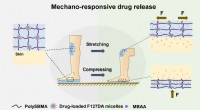
- Mechano-responsieve hydrogel ontwikkeld voor wondgenezing
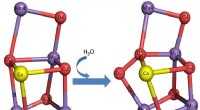
- Innovatieve fotokatalytische materialen van koolstofnanobuisjes voor efficiënte omzetting van zonne-energie en waterstofproductie
- Betere en goedkopere zorg met droge bloedmonsters

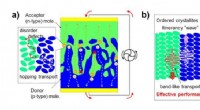
- Ladingsdragers volgen in het moleculaire kristal op organische pn-junctie
 Onderzoekers ontdekken de echte reden waarom schildpadden schelpen hebben
Onderzoekers ontdekken de echte reden waarom schildpadden schelpen hebben  Risico op meerdere klimaatomslagpunten escaleert boven 1,5°C opwarming van de aarde
Risico op meerdere klimaatomslagpunten escaleert boven 1,5°C opwarming van de aarde Instortende ster baart een zwart gat
Instortende ster baart een zwart gat Bomen in dit biome werpen hun bladeren af. De herfsttemperatuur varieert met seizoenen is de?
Bomen in dit biome werpen hun bladeren af. De herfsttemperatuur varieert met seizoenen is de?  Wanneer consumenten een chatbot verkiezen boven een persoon
Wanneer consumenten een chatbot verkiezen boven een persoon  Hoe lang was de eerste reis naar de maan?
Hoe lang was de eerste reis naar de maan?  In de trage Russische economie, halal ziet groei
In de trage Russische economie, halal ziet groei Botsingsresonanties tussen ultrakoud atoom en moleculen voor het eerst gevisualiseerd
Botsingsresonanties tussen ultrakoud atoom en moleculen voor het eerst gevisualiseerd
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

