
Wetenschap
Wat toont de relatie tussen reactanten en producten in een chemische reactie?
Hier is hoe het werkt:
* reactanten: Dit zijn de stoffen die aanwezig zijn aan het begin van een chemische reactie. Ze zijn geschreven aan de linkerkant van de vergelijking.
* Producten: Dit zijn de stoffen die worden gevormd als gevolg van de chemische reactie. Ze zijn geschreven aan de rechterzijde van de vergelijking.
* pijl: Een pijl scheidt de reactanten van de producten, wat de richting van de reactie aangeeft.
Bijvoorbeeld:
reactanten → producten
2h₂ + o₂ → 2h₂o
Deze vergelijking toont aan dat twee moleculen waterstofgas (H₂) reageren met één molecuul zuurstofgas (O₂) om twee watermoleculen te produceren (H₂O).
Belangrijke kenmerken van een chemische vergelijking:
* coëfficiënten: Dit zijn de getallen die voor elke chemische formule worden geplaatst om de vergelijking in evenwicht te brengen. Ze geven het relatieve aantal mol aan van elke reactant en product.
* staten van materie: Subscripts kunnen tussen haakjes worden toegevoegd om de toestand van materie van elke stof aan te geven (bijv. (S) voor vaste, (l) voor vloeistof, (g) voor gas, (aq) voor waterige oplossing).
Naast de chemische vergelijking kunnen andere representaties ook de relatie tussen reactanten en producten aantonen:
* reactiemechanismen: Deze beschrijven het stapsgewijze proces van een chemische reactie, die de vorming van tussenproducten en overgangstoestanden tonen.
* Energiediagrammen: Deze visualiseren de energieveranderingen die betrokken zijn bij een reactie, die de relatieve energieën van reactanten, producten en eventuele tussenproducten tonen.
Inzicht in de relatie tussen reactanten en producten is cruciaal voor het begrijpen van de fundamentele principes van chemie en voor het voorspellen en beheersen van chemische reacties.
 NASA kijkt naar de grote waterdampconcentratie van orkaan Rosas
NASA kijkt naar de grote waterdampconcentratie van orkaan Rosas Nieuw bewijs wijst op groeiende stedelijke watercrisis
Nieuw bewijs wijst op groeiende stedelijke watercrisis Met een daling van LA's vervuiling door aerosolen, vegetatie komt naar voren als belangrijke bron
Met een daling van LA's vervuiling door aerosolen, vegetatie komt naar voren als belangrijke bron Onderzoekers ontwikkelen nieuwe verklaring voor destructieve aardbevingstrillingen
Onderzoekers ontwikkelen nieuwe verklaring voor destructieve aardbevingstrillingen Chinese stad annuleert vluchten in 2e dag van smogalarm
Chinese stad annuleert vluchten in 2e dag van smogalarm
Hoofdlijnen
- Verbetering van de kwaliteitsanalyse van zoete aardappel met hyperspectrale beeldvorming en AI
- Welk weefsel is verantwoordelijk voor het uitvoeren van opgeloste voedselstoffen?
- Waar zijn hormonen een voorbeeld van?
- Wat zijn de drie belangrijkste spieren in het menselijk lichaam?
- Wat is calyptra in de plantkunde?
- Biologen onthullen hoe obesitas het skeletspiermetabolisme schaadt
- Hoe tardigrades vriestemperaturen overleven
- Facebook laat gebruikers, net als MySpace, de volledige naam weergeven
- Wat zijn de sterke punten van de biogenesetheorie?
- Wetenschappers ontwikkelen krachtige familie van 2D-materialen

- Big data-techniek onthult voorheen onbekende mogelijkheden van veelgebruikte materialen

- Onderzoekers zetten niet-giftige resten om in coating die slijtvast is, vlek en zonlicht

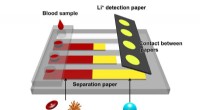
- Nieuw apparaat detecteert snel lithiumionen in bloed van patiënten met bipolaire stoornis
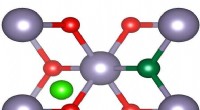
- Discovery wijst de weg naar betere en goedkopere transparante geleiders
 Drie donkere velden voor Euclids diep onderzoek
Drie donkere velden voor Euclids diep onderzoek Wat verwijst naar sedimenten die zijn afgezet van stromen?
Wat verwijst naar sedimenten die zijn afgezet van stromen?  Wat voor soort organismen veroorzaken dinitrificatie?
Wat voor soort organismen veroorzaken dinitrificatie?  Waarom wordt het snijden van kalk beschouwd als een chemische verandering?
Waarom wordt het snijden van kalk beschouwd als een chemische verandering?  Liter omrekenen in kilogram bij het berekenen van massa
Liter omrekenen in kilogram bij het berekenen van massa Hoe organische magneten groeien in een dunne film
Hoe organische magneten groeien in een dunne film  Expert bespreekt social distancing en cyberpesten
Expert bespreekt social distancing en cyberpesten Lijst met celorganellen en hun functies
Lijst met celorganellen en hun functies
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

