
Wetenschap
Wanneer zout in water wordt opgelost, dissociëren de natrium- en chloride -ionen?
* ionische verbindingen: Zout is een ionische verbinding, wat betekent dat deze wordt gevormd door de elektrostatische aantrekkingskracht tussen positief geladen natriumionen (Na+) en negatief geladen chloride-ionen (Cl-).
* Polaire watermoleculen: Water is een polair molecuul, wat betekent dat het een enigszins positief uiteinde heeft (nabij de waterstofatomen) en een enigszins negatief uiteinde (nabij het zuurstofatoom).
* dissociatie: Wanneer zout aan water wordt toegevoegd, omringen de polaire watermoleculen de Na+ en Clers. De positieve uiteinden van watermoleculen worden aangetrokken door de negatieve chloride -ionen en de negatieve uiteinden van watermoleculen worden aangetrokken door de positieve natriumionen. Deze aantrekkingskracht overwint de elektrostatische kracht die de ionen bij elkaar houdt in het zoutkristal, waardoor de ionen scheiden (dissociëren) en omringd worden door watermoleculen.
Samenvattend: Het oplossen van zout in water is een proces van dissociatie , waarbij de ionische bindingen tussen natrium- en chloride-ionen worden verbroken door de aantrekkingskracht van polaire watermoleculen, wat resulteert in vrije Na+ en clionen in oplossing.
 De reactiesnelheid van een gegeven reactant of product delen door zijn stoichiometrische coëfficiënt?
De reactiesnelheid van een gegeven reactant of product delen door zijn stoichiometrische coëfficiënt?  Hoe worden wassen gemaakt?
Hoe worden wassen gemaakt?  Bacteriën aangeworven in Franse strijd voor autonomie van zeldzame aardmetalen
Bacteriën aangeworven in Franse strijd voor autonomie van zeldzame aardmetalen Kristallijne kunstmatige spier zorgt ervoor dat papieren pop sit-ups doet
Kristallijne kunstmatige spier zorgt ervoor dat papieren pop sit-ups doet Is het breken van een potlood een halve chemische verandering?
Is het breken van een potlood een halve chemische verandering?
 Experts ontdekken de water- en emissievoetafdruk van sneeuwkanonnen:kunnen we erop vertrouwen in een tijdperk van klimaatverandering?
Experts ontdekken de water- en emissievoetafdruk van sneeuwkanonnen:kunnen we erop vertrouwen in een tijdperk van klimaatverandering?  Storing afvalwaterzuiveringsinstallatie Warschau vervuilt rivier Wisla
Storing afvalwaterzuiveringsinstallatie Warschau vervuilt rivier Wisla Hoe lang bestaat de aarde al?
Hoe lang bestaat de aarde al?  Weerbaarheid tegen klimaatverandering Samoa stelt westerse percepties op de proef
Weerbaarheid tegen klimaatverandering Samoa stelt westerse percepties op de proef Video:Wetenschappers onderzoeken oceaanstromingen door middel van supercomputersimulaties
Video:Wetenschappers onderzoeken oceaanstromingen door middel van supercomputersimulaties
Hoofdlijnen
- Wat maakt het maken van een echt eiwit?
- Wat is opgenomen in de wetenschap?
- Hoe verwerven cellen homologe chromosoomparen die de allelen dragen, onafhankelijk diverteren?
- Een nieuwe strategie om cold case-onderzoeken te versnellen
- Kunnen herten aanwijzingen bevatten over het verband tussen malariaresistentie en sikkelcelziekte?
- Sterven bacteriën ooit uit? Nieuw onderzoek zegt ja, groots
- Hebben mannen en vrouwen verschillende hersenen?
- Tijm tussen amandelbomen verzacht de klimaatverandering en verhoogt de landproductie
- Naast twee sekschromossomen hebben mensen 44 andere chromosomen genoemd?
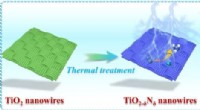
- Surface defect engineering van nanodraadarrays naar efficiënte stikstofreductie voor ammoniaksynthese
- Speciale eiwitrijke planten zorgen voor eiwitten, vezels en antioxidanten in één verpakking

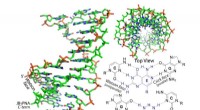
- Synthetisch molecuul dringt dubbelstrengs DNA binnen
- Bloed van drugsgebruikers kan herkomst van drugs onthullen

- Molecuul uit de natuur zorgt voor volledig recyclebare polymeren

 Hoe heet het membraan dat de ene cel van de andere scheidt?
Hoe heet het membraan dat de ene cel van de andere scheidt?  Hoe verliezen orkanen energie?
Hoe verliezen orkanen energie?  Bereken het procentuele verschil met drie sommen
Bereken het procentuele verschil met drie sommen  NASA schat de regenval van de tropische storm Sebastiens
NASA schat de regenval van de tropische storm Sebastiens JRC-analyse helpt reactie op instorting van de dam in Laos
JRC-analyse helpt reactie op instorting van de dam in Laos Open cluster NGC 2158 in detail onderzocht
Open cluster NGC 2158 in detail onderzocht Wat weegt een gallon ijzerchloride?
Wat weegt een gallon ijzerchloride?  Honderdjarige stormen? Zo lang duren ze op Saturnus
Honderdjarige stormen? Zo lang duren ze op Saturnus
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

