
Wetenschap
Wat is de elektronenconfiguratie voor koper?
[AR] 3D¹⁰ 4S¹
Dit is waarom dit het geval is:
* [AR] Vertegenwoordigt de elektronenconfiguratie van argon, het edelgas dat voorafgaat aan koper op het periodieke tabel. Dit betekent dat koper dezelfde innerlijke elektronenconfiguratie heeft als argon.
* 3d¹⁰ Geeft aan dat de 3D -subshell volledig gevuld is met 10 elektronen.
* 4S¹ Geeft aan dat de 4S -subshell slechts één elektron heeft.
Waarom niet [AR] 3D⁹ 4S²?
U kunt verwachten dat koper deze configuratie heeft op basis van de standaard vulvolgorde. Een volledig gevulde D -subshell is echter stabieler dan een gedeeltelijk gevulde. De extra stabiliteit die wordt verkregen door een volledige 3D -subshell te hebben, weegt zwaarder dan het lichte energie -nadeel van het hebben van slechts één elektron in de 4S -subshell.
 Meten en modelleren van methaanemissies in wetlands
Meten en modelleren van methaanemissies in wetlands  Materie verandert hoe het eruit ziet, maar niet wat er van is gemaakt?
Materie verandert hoe het eruit ziet, maar niet wat er van is gemaakt?  Een Californische vulkaan vernietigde ooit een bos en stuwde as 280 mijl voort. Experts zeggen dat het een waarschuwing biedt
Een Californische vulkaan vernietigde ooit een bos en stuwde as 280 mijl voort. Experts zeggen dat het een waarschuwing biedt Kies voor hoop of klimaatovergave, zegt VN-chef
Kies voor hoop of klimaatovergave, zegt VN-chef Hoe verandert de wetenschap de wereld?
Hoe verandert de wetenschap de wereld?
Hoofdlijnen
- Welke membraaneiwitten is verantwoordelijk voor het binden van hormonen die veranderingen in de activiteit van de cellen kunnen activeren?
- Wat hebben mitochondirale en thylakoïde membranen gemeen?
- Waarom zijn planten nodig voor het overleven van alle dieren op aarde en waarom?
- Welke functies dienen displays en rituelen op dieren?
- Hoe plantensensoren ziekteverwekkers detecteren
- Kan een vrouwelijke plant alleen zaden produceren?
- Wat is hoogstwaarschijnlijk te vinden in een eencellig en multicellulair organisme?
- Hoeveel organen heeft een dierencel?
- Hoe zeewiervretende krabben koraalriffen kunnen helpen redden
- Chemisch waterstofopslagsysteem
- Koffievervalsing ontdekt met nieuwe methode

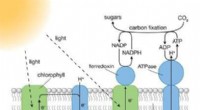
- Wetenschappers ontwerpen moleculair systeem voor kunstmatige fotosynthese
- Universele latente aniondonoren voor ultralage werkfunctie-oplossing-verwerkbare elektroden

- Pulsen van een atoomscherpe punt stellen onderzoekers in staat om naar believen chemische bindingen te verbreken en te vormen

 Wat is een synoniem voor verplicht?
Wat is een synoniem voor verplicht?  Hoe beïnvloedt zonlicht het vermogen van planten om te overleven?
Hoe beïnvloedt zonlicht het vermogen van planten om te overleven?  Welke apparaten gebruiken 13 versterkers?
Welke apparaten gebruiken 13 versterkers?  De manen van Jupiter kunnen elkaar opwarmen
De manen van Jupiter kunnen elkaar opwarmen Wat is vaste macrofaag?
Wat is vaste macrofaag?  Laser verbetert de tijdresolutie van CryoEM
Laser verbetert de tijdresolutie van CryoEM De oceaan reageert op een opwarmende planeet
De oceaan reageert op een opwarmende planeet Heeft het oppervlak van de maan bergen en kraters?
Heeft het oppervlak van de maan bergen en kraters?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

