
Wetenschap
Waarom kan een zuurstofatoom geen drievoudige binding vormen?
* valentie -elektronen: Zuurstof heeft zes valentie -elektronen (elektronen in de buitenste schaal). Om een stabiele octetconfiguratie te bereiken, moet het nog twee elektronen krijgen.
* bindingscapaciteit: Elke covalente binding omvat het delen van twee elektronen. Zuurstof kan maximaal twee covalente bindingen vormen, met behulp van zijn twee ongepaarde valentie -elektronen.
* geen lege orbitalen: De P-orbitalen van Oxygen zijn allemaal gevuld met elektronen. Er zijn geen lege orbitalen beschikbaar voor het vormen van extra obligaties.
* afstoting: Drievoudige bindingen omvatten een significante elektronendichtheid in het bindingsgebied. De afstoting tussen de elektronen in een drievoudige binding zou te hoog zijn voor het kleine formaat van Oxygen om te huisvesten.
Samenvattend: De elektronenconfiguratie en beperkte bindingscapaciteit van Oxygen voorkomen dat het drievoudige bindingen vormt.
 Welke metalen reageren met zuur om waterstof te produceren?
Welke metalen reageren met zuur om waterstof te produceren?  Een nieuwe katalysator voor watersplitsing die het beste van twee werelden is
Een nieuwe katalysator voor watersplitsing die het beste van twee werelden is Chemische neus snuffelt kritische verschillen in DNA-structuren
Chemische neus snuffelt kritische verschillen in DNA-structuren Nieuwe materialen vertonen een gespleten persoonlijkheid
Nieuwe materialen vertonen een gespleten persoonlijkheid Welke chemische vergelijking voor de verbranding van fossiele brandstoffen Apex?
Welke chemische vergelijking voor de verbranding van fossiele brandstoffen Apex?
 Hoe meerdere factoren van klimaatverandering de bodem beïnvloeden
Hoe meerdere factoren van klimaatverandering de bodem beïnvloeden  Australië beleeft warmste dag ooit
Australië beleeft warmste dag ooit Wildvuur in Nieuw-Zeeland zal naar verwachting wekenlang branden
Wildvuur in Nieuw-Zeeland zal naar verwachting wekenlang branden Overstromingen en tranen in Bangladesh een week na cycloon
Overstromingen en tranen in Bangladesh een week na cycloon Bodemschimmels kunnen helpen bij het bepalen van de veerkracht van bossen tegen veranderingen in het milieu
Bodemschimmels kunnen helpen bij het bepalen van de veerkracht van bossen tegen veranderingen in het milieu
Hoofdlijnen
- Welk orgaansysteem verplaatst geen materialen in het lichaam?
- De structuur en functie van ribosomen in eukaryoten en prokaryoten
- DNA van een Incajongen die 500 jaar geleden werd geofferd, laat zien hoe mensen zich naar Zuid-Amerika verspreidden
- Nieuwe eDNA-methode opent deuren voor milieuonderzoek
- Waar bevinden zich delen van het chloroplast-ATP-synthase die betrokken zijn bij de fosforylering van ADP naar ATP?
- Waarom zou Wegener een interdisciplinaire wetenschapper kunnen worden genoemd, de wetenschapsvelden identificeren die hij goed geïnformeerd was?
- Tonen dieren bewustzijn? | Hoe dingen werken
- Ecologische impact van eucalyptusbomen:balans tussen voordelen en risico's
- Hoe heet het enzym dat nieuwe nucleotiden correct aan de open DNA-streng hecht?
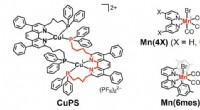
- Grote stappen voor het vastleggen van koolstof met behulp van aarde-overvloedige elementen als fotokatalytisch systeem
- Chemici ontdekken dat watermicrodruppeltjes spontaan waterstofperoxide produceren

- Zelfaangedreven papierchips kunnen helpen om vroegtijdig alarm te slaan voor bosbranden

- Wetenschappers ontwikkelen voorspellingsmodel voor bellendiameter voor industrieel gebruik

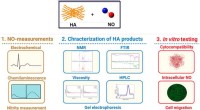
- Onderzoekers gebruiken stikstofmonoxidevangers om triple-negatieve borstkanker aan te pakken
 Heiligdom aan de kant van de Mexicaanse vulkaan zou een universummodel kunnen zijn
Heiligdom aan de kant van de Mexicaanse vulkaan zou een universummodel kunnen zijn EU-leiders beloven harde actie tegen cyberaanvallen
EU-leiders beloven harde actie tegen cyberaanvallen Zijn we alleen? De vraag is een serieuze wetenschappelijke studie waard
Zijn we alleen? De vraag is een serieuze wetenschappelijke studie waard Nagemaakte en door piraterij verkregen goederen vertegenwoordigen 3,3% van de wereldhandel:rapport
Nagemaakte en door piraterij verkregen goederen vertegenwoordigen 3,3% van de wereldhandel:rapport Uit onderzoek blijkt hoeveel CEO's belangrijk zijn voor de prestaties van een bedrijf
Uit onderzoek blijkt hoeveel CEO's belangrijk zijn voor de prestaties van een bedrijf Hoe ervoor te zorgen dat biodiversiteitsgegevens EERLIJK, gekoppeld, open en toekomstbestendig zijn
Hoe ervoor te zorgen dat biodiversiteitsgegevens EERLIJK, gekoppeld, open en toekomstbestendig zijn  Energie-efficiënte fotochemie op zonne-energie met luminescente zonneconcentratoren
Energie-efficiënte fotochemie op zonne-energie met luminescente zonneconcentratoren Wat zijn de 3 lagen zon?
Wat zijn de 3 lagen zon?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

