
Wetenschap
Wat is de chemische reactie van natriumsulfiet en water?
Hier is de chemische vergelijking voor de reactie:
na₂so₃ (aq) + h₂o (l) ⇌ 2na⁺ (aq) + so₃²⁻ (aq) + h₂o (l)
Verklaring:
* Natriumsulfiet (Na₂so₃) Lost in water op om natriumionen (Na⁺) en sulfietionen (SO₃²⁻) te vormen.
* sulfite -ionen (So₃²⁻) zijn de conjugaatbasis van het zwakke zuur, bisulfiet -ion (HSO₃⁻). Ze reageren met watermoleculen om bisulfietionen (HSE₃⁻) en hydroxide -ionen te vormen (OH⁻).
* Hydroxide -ionen (oh⁻) Maak de oplossing enigszins eenvoudig.
Algemene reactie:
De algehele reactie kan worden vereenvoudigd als:
so₃²⁻ (aq) + h₂o (l) ⇌ hso₃⁻ (aq) + oh⁻ (aq)
Belangrijke opmerking:
De reactie is een evenwicht reactie. Dit betekent dat de reactie in beide richtingen verloopt, waarbij de voorwaartse reactie enigszins de voorkeur heeft. Als gevolg hiervan zal de oplossing enigszins eenvoudig zijn, maar niet sterk.
 Wetenschappers werpen nieuw licht op de rol van virussen bij koraalverbleking
Wetenschappers werpen nieuw licht op de rol van virussen bij koraalverbleking Extreme hitte veroorzaakt bosbranden in Chili, waarbij minstens 51 doden vallen
Extreme hitte veroorzaakt bosbranden in Chili, waarbij minstens 51 doden vallen  Grootste studie ooit van koraalgemeenschappen ontgrendelt wereldwijde oplossing om riffen te redden
Grootste studie ooit van koraalgemeenschappen ontgrendelt wereldwijde oplossing om riffen te redden Schildpadvriendelijk plastic? Een slimme oplossing voor vervuiling, stroperij en armoede
Schildpadvriendelijk plastic? Een slimme oplossing voor vervuiling, stroperij en armoede  Lossen sneeuwbalstruiken in de herfst los?
Lossen sneeuwbalstruiken in de herfst los?
Hoofdlijnen
- Welke niet-levende wezens bestuderen mariene biologen?
- Wat zijn verschillende soorten refferatie?
- Wat is de organel die krachtpatser van de cel?
- Wat is een wetenschappelijk idee?
- Welke factoren beïnvloeden de scheiding van stoffen in kolomchromatogafie?
- Onderzoek onthult opmerkelijke variabiliteit in de hittetolerantie van koraal
- Wat wordt het proces genoemd door welke macromeculen worden gevormd?
- Welke factor heeft geen invloed op de enzymfunctie?
- Toyocamycine-opnamewijze ontdekt:goed nieuws voor de ontwikkeling van antischimmelmiddelen
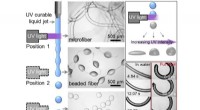
- Oogsten van microdeeltjes uit een vloeistofstraal
- Nieuwe klasse katalysatoren voor energieconversie

- Onderzoekers lopen voorop bij het ontwikkelen van machine learning-methoden voor chemische ontdekking
- Onderzoekers vinden een manier om het hele spectrum van zonlicht te benutten

- Onderzoeksteam helpt Arcteryx groen en droog te blijven met waterafstotende stoffen van de volgende generatie

 Verbergend zwart gat gevonden
Verbergend zwart gat gevonden Wat gebeurde wanneer natriumchloride reageert met zoutzuur?
Wat gebeurde wanneer natriumchloride reageert met zoutzuur?  Astronaut Buzz Aldrin rolt de rode loper uit voor Mars (update)
Astronaut Buzz Aldrin rolt de rode loper uit voor Mars (update) Onderzoek laat zien hoe verschillen in mannelijke en vrouwelijke hersenen ontstaan
Onderzoek laat zien hoe verschillen in mannelijke en vrouwelijke hersenen ontstaan  Onderzoekers onthullen hoe een belangrijk weersysteem in Noordoost-China wordt gemoduleerd door El Niño
Onderzoekers onthullen hoe een belangrijk weersysteem in Noordoost-China wordt gemoduleerd door El Niño  Grafeen brengt kwantumeffecten naar elektronische circuits
Grafeen brengt kwantumeffecten naar elektronische circuits Een nieuwe grens op axions
Een nieuwe grens op axions Synergetische samenwerking leidt tot nieuwe strategie voor biomedische 3D-beeldvorming
Synergetische samenwerking leidt tot nieuwe strategie voor biomedische 3D-beeldvorming
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

