
Wetenschap
Waarom zou waterstof bestaan als een molecuul?
* Elektronische configuratie: Elk waterstofatoom heeft slechts één proton en één elektron. Het heeft twee elektronen nodig om een stabiele, edelgasconfiguratie zoals helium te bereiken.
* Bondvorming: Om stabiliteit te bereiken, delen twee waterstofatomen hun enkele elektronen, waardoor een covalente binding wordt gevormd . Dit gedeelde paar elektronen vult beide buitenste schalen van beide atomen, waardoor ze stabieler worden.
Voordelen van het vormen van H₂:
* Verhoogde stabiliteit: Het molecuul is stabieler dan individuele waterstofatomen.
* Lagere energie: De gedeelde elektronen resulteren in een lagere energietoestand voor het systeem, waardoor het molecuul stabieler wordt.
Samenvattend: Waterstof bestaat als een molecuul omdat het een stabielere en lagere energie-configuratie is dan individuele atomen. Dit komt door het delen van elektronen door een covalente binding, het vervullen van de behoefte aan een complete buitenste schaal en het bereiken van een stabiele, edelgasconfiguratie.
 Hoe plastic-etende bacteriën eigenlijk werken - legt een chemicus uit
Hoe plastic-etende bacteriën eigenlijk werken - legt een chemicus uit Een doorbraak in katalysatoren:kleiner dan nanoschaal
Een doorbraak in katalysatoren:kleiner dan nanoschaal Hoe wordt een uranium-235-kern gemaakt om splijting te ondergaan?
Hoe wordt een uranium-235-kern gemaakt om splijting te ondergaan?  Ongebalanceerde vergelijking voor vast zink plus zuurstof levert II-oxide op?
Ongebalanceerde vergelijking voor vast zink plus zuurstof levert II-oxide op?  Welk experiment overtuigde Ernest Rutherford dat het atoom een kleine positiviteitskleur heeft?
Welk experiment overtuigde Ernest Rutherford dat het atoom een kleine positiviteitskleur heeft?
 Wat ligt er onder smeltende gletsjers en ontdooiende permafrost?
Wat ligt er onder smeltende gletsjers en ontdooiende permafrost? EPA maakt Californische voorgestelde verbod op nieuwe gasauto's belachelijk
EPA maakt Californische voorgestelde verbod op nieuwe gasauto's belachelijk Klimaat:welke landen en steden lopen het grootste risico?
Klimaat:welke landen en steden lopen het grootste risico?  Moerasmicrobe heeft een vervuilende kracht
Moerasmicrobe heeft een vervuilende kracht Californias cap-and-trade luchtkwaliteitsvoordelen gaan meestal uit de staat
Californias cap-and-trade luchtkwaliteitsvoordelen gaan meestal uit de staat
Hoofdlijnen
- Hoe coördineren cellen hun gedrag met anderen om gedrag op weefselschaal te creëren?
- Welke structuur in een cel bestaat voornamelijk uit fosfolipide dubbellaag?
- Verkeerd gelabeld haaienvlees is wijdverbreid op de Australische markten, zo blijkt uit onderzoek
- Wat zijn de twee soorten nucleïnezuur hun functies?
- Waar verzamelt wetenschapper kennis op?
- Waarom evolutie vaak de voorkeur geeft aan kleine dieren en andere organismen
- Waarom hebben meristematische cellen grote kernen?
- Welke oplossing veroorzaakt osmose?
- Wat is de Latijnse naam van Lobelia -fabriek?
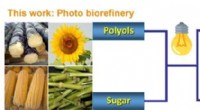
- Nieuwe fotokatalytische methode zet biopolyolen en suikers om in methanol en syngas
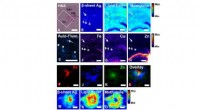
- Gecombineerde beeldvormingsbenadering karakteriseert plaques geassocieerd met de ziekte van Alzheimer
- Een opschaalbare nanoporeuze membraancentrifuge voor ontzilting door omgekeerde osmose zonder vervuiling

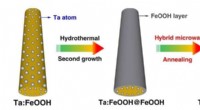
- Een stap dichter bij praktische zonne-waterstofproductie via uitgebreid gemodificeerde hematiet-fotoanode
- Hoe bacteriën mangaanoxide nanodeeltjes produceren

 Wetenschappers:Verrassend kleine dode zone bij Louisiana
Wetenschappers:Verrassend kleine dode zone bij Louisiana Lab ontsluit geheimen van 3D-printen op nanoschaal
Lab ontsluit geheimen van 3D-printen op nanoschaal Hoe om RPM naar MPH te converteren met een rekenmachine
Hoe om RPM naar MPH te converteren met een rekenmachine Welke maat voor de atmosfeer vertelt ons hoeveel vibratie -energie lucht bevat per massa -eenheid?
Welke maat voor de atmosfeer vertelt ons hoeveel vibratie -energie lucht bevat per massa -eenheid?  Sewall Green Wright
Sewall Green Wright  AI-aangedreven elektronische neus om de versheid van vlees te ruiken
AI-aangedreven elektronische neus om de versheid van vlees te ruiken Onderzoekers vestigen zonnerecord met next-gen cellen
Onderzoekers vestigen zonnerecord met next-gen cellen De overdracht van genen tijdens bacteriële conjugatie omvat rigide buisvormige aanhangsels met de naam Wat?
De overdracht van genen tijdens bacteriële conjugatie omvat rigide buisvormige aanhangsels met de naam Wat?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

