
Wetenschap
Wat maakt het ene atoom of element anders dan het andere?
* atomen zijn de kleinste eenheid van een chemisch element dat kan bestaan. Ze zijn samengesteld uit een kern die protonen en neutronen bevat, omgeven door een wolk van elektronen.
* elementen zijn pure stoffen bestaande uit slechts één type atoom. Dit betekent dat alle atomen in een element hetzelfde aantal protonen hebben. Alle gouden atomen hebben bijvoorbeeld 79 protonen, terwijl alle zuurstofatomen 8 protonen hebben.
Hier is een uitsplitsing van wat atomen van verschillende elementen anders maken:
1. Atomisch nummer (aantal protonen):
* Dit is het bepalende kenmerk van een element.
* Het aantal protonen in de kern van een atoom bepaalt het atoomnummer.
* Elementen worden op het periodieke tabel gerangschikt door het atoomnummer te vergroten.
2. Aantal neutronen:
* Atomen van hetzelfde element kunnen verschillende aantallen neutronen hebben. Dit worden isotopen genoemd.
* Isotopen van een element hebben dezelfde chemische eigenschappen omdat ze hetzelfde aantal protonen en elektronen hebben.
* Bijvoorbeeld, koolstof-12 en koolstof-14 zijn isotopen van koolstof, beide met 6 protonen maar verschillen in neutronenaantallen (respectievelijk 6 en 8).
3. Aantal elektronen:
* Atomen zijn typisch neutraal, wat betekent dat ze een gelijk aantal protonen en elektronen hebben.
* Atomen kunnen echter elektronen winnen of verliezen, waardoor ionen worden gevormd. Dit verandert de lading van het atoom maar verandert niet het atoomnummer (aantal protonen).
Samenvattend:
Het aantal protonen (atoomnummer) is het fundamentele verschil tussen atomen van verschillende elementen. Dit nummer bepaalt de identiteit van het element en het chemische gedrag ervan. Hoewel het aantal neutronen en elektronen kan variëren, veranderen ze de identiteit van het element niet.
 Tropische vissenspeeltuin in Belize kaatst terug van bedreigingen (update)
Tropische vissenspeeltuin in Belize kaatst terug van bedreigingen (update) Bomen in de uiterwaarden van de Amazone stoten evenveel methaan uit als alle oceanen van de aarde samen
Bomen in de uiterwaarden van de Amazone stoten evenveel methaan uit als alle oceanen van de aarde samen Machine learning gebruiken om dode zones in meren te modelleren
Machine learning gebruiken om dode zones in meren te modelleren  Chemische cocktail gevonden in Barrier Reef-schildpadden
Chemische cocktail gevonden in Barrier Reef-schildpadden Modderige wateren:zinkende organische stoffen veranderen zeebodemrecords
Modderige wateren:zinkende organische stoffen veranderen zeebodemrecords
Hoofdlijnen
- Alle in Michigan bevestigde poema's waren mannelijk:waarom we geen vrouwtjes en kittens zien
- Wat is pleoitophs?
- Elk menselijk gen is gesequenced als gevolg van wat?
- 380 miljoen jaar oud hart verlicht evolutionaire geschiedenis
- Difference Between Gap Junctions & Plasmodesmata
- Welk type moleculen komen ten minste drie binnen de cel via passieve transportlijst?
- Nieuw inzicht in hoe bijen zien
- Wat is de naam van het proces waar ATP is gemaakt van voedselmoleculen?
- Welke soorten dieren eten balpythons?
- 3D-geprint voedsel opscheppen, één smakelijke afdruk per keer

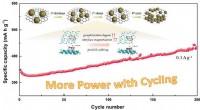
- Verfijning van deeltjes induceert en verhoogt de cycluscapaciteit van natrium/lithium-ionbatterijen
- Snel reagerend, kleurveranderende moleculaire sonde detecteert wanneer een materiaal op het punt staat te falen

- Lasertechnieken en fotochemie vinden ongrijpbare moleculaire bouwsteen
- Wetenschappers bij ESS, Zweeds wateronderzoek, ORNL gebruikt VISION om te kijken naar veelvoorkomende verontreinigingen voor toepassingen in schoner water

 Is de zon hoog of laag in Sky Groot -Brittannië?
Is de zon hoog of laag in Sky Groot -Brittannië?  Wat was de grootste komeet ooit om de aarde te raken?
Wat was de grootste komeet ooit om de aarde te raken?  Video:Vlucht over de Korolev-krater op Mars
Video:Vlucht over de Korolev-krater op Mars Team maakt jacht op de planeet een groepsinspanning, vindt meer dan 100 kandidaten
Team maakt jacht op de planeet een groepsinspanning, vindt meer dan 100 kandidaten Wat is de betekenis van de maan tijdens een zonsopgang?
Wat is de betekenis van de maan tijdens een zonsopgang?  Kunstmatige vinger die oppervlaktemateriaal kan identificeren met een nauwkeurigheid van 90%
Kunstmatige vinger die oppervlaktemateriaal kan identificeren met een nauwkeurigheid van 90% Aardgaspijpleidingen onder druk zetten voor lekkagedetectie
Aardgaspijpleidingen onder druk zetten voor lekkagedetectie  De Finnøy ijsbeer
De Finnøy ijsbeer
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

