
Wetenschap
Waarom heeft Boron een hogere ionisatie -energie dan fluor?
Dit is waarom:
* ionisatie -energie is de energie die nodig is om een elektron uit een atoom in zijn gasvormige toestand te verwijderen.
* elektronegativiteit is een maat voor het vermogen van een atoom om elektronen aan te trekken.
Fluor is veel elektronegatiefer dan boor. Dit betekent dat de elektronen van fluor strakker worden gehouden ten opzichte van de kern, waardoor het moeilijker is om een elektron te verwijderen. Dit leidt tot een hogere ionisatie -energie.
Waarom zou iemand denken dat Boron een hogere ionisatie -energie heeft?
Ze denken misschien aan de algemene trend in ionisatie -energie gedurende een periode:
* ionisatie -energie neemt over het algemeen toe gedurende een periode Vanwege de toenemende nucleaire lading en afnemende atoomradius. Dit betekent dat elektronen steviger worden gehouden als u van links naar rechts over het periodiek systeem gaat.
Deze trend is echter niet altijd perfect lineair. Fluor is een uitzondering vanwege de extreem hoge elektronegativiteit. Dit overschrijft de algemene trend gedurende de periode, waardoor het de hoogste ionisatie -energie van alle elementen heeft.
Laat het me weten als je nog andere vragen hebt!
Hoofdlijnen
- Het leven is mooi voor de imkers in Griekenland, maar hoe lang?
- De effectiviteit van camouflage bij verschillende dieren vergelijken
- Hoe reproduceert een zebravissen zich?
- Systeem dat reproductie mogelijk maakt en mannelijke vrouwelijke functies in staat stelt?
- Bestaat er een verband tussen intelligentie en psychische aandoeningen?
- Genetici lossen een veertig jaar oud dilemma op om te verklaren waarom dubbele genen in het genoom achterblijven
- Wetenschappers ontdekken nieuwe informatie over hoe enzymen uit witte bloedcellen functioneren
- Hoe lokale ecologische kennis bedreigde en zeldzame dieren kan redden
- Welke structuur in het urinestelsel is het belangrijkst?
- Celdoodblokker voorkomt dat gezonde cellen afsterven

- Nieuw apparaat kan warmte-energie omzetten in een levensvatbare brandstofbron
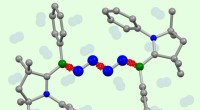
- Inerte stikstof gedwongen om met zichzelf te reageren
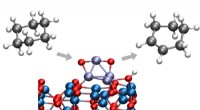
- Wetenschappers pionieren met nieuw chemisch conversieproces bij lage temperatuur
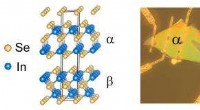
- Plasma-elektronen kunnen worden gebruikt om metaalfilms te produceren

 Klimaatvragen:wat zijn de oplossingen voor klimaatverandering?
Klimaatvragen:wat zijn de oplossingen voor klimaatverandering?  Is het vermogen om metalen op te lossen een fysische of chemische eigenschap?
Is het vermogen om metalen op te lossen een fysische of chemische eigenschap?  Welke stoffen en chemicaliën zijn betrokken bij broeikasgassen?
Welke stoffen en chemicaliën zijn betrokken bij broeikasgassen?  Kun je je mobiele telefoonlader in Europa gebruiken met een spanningsconverter voor apparaten van 500-1600 watt?
Kun je je mobiele telefoonlader in Europa gebruiken met een spanningsconverter voor apparaten van 500-1600 watt?  De massa van een vloeistof vinden
De massa van een vloeistof vinden Hoe wordt methylparaben gemaakt?
Hoe wordt methylparaben gemaakt?  Ionenstraaltherapie modelleren
Ionenstraaltherapie modelleren Kwantumsystemen corrigeren zichzelf
Kwantumsystemen corrigeren zichzelf
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


