
Wetenschap
Waarom zijn vaste stoffen betere warmtegeleiders dan gassen?
1. Deeltjesafstand:
* vaste stoffen: Deeltjes in vaste stoffen zijn strak gepakt, met zeer weinig ruimte ertussen.
* gassen: Deeltjes in gassen zijn op grote schaal verdeeld en bewegen vrij.
2. Deeltjesinteracties:
* vaste stoffen: De nabijheid van deeltjes in vaste stoffen leidt tot sterke intermoleculaire krachten, zoals ionische bindingen, metalen bindingen of covalente bindingen. Deze krachten beperken deeltjesbeweging en zorgen voor een efficiënte energieoverdracht.
* gassen: Door de zwakke intermoleculaire krachten in gassen kunnen deeltjes vrij vaak bewegen en minder vaak botsen.
3. Energieoverdrachtsmechanismen:
* vaste stoffen: Warmteoverdracht in vaste stoffen treedt voornamelijk op door geleiding , waar vibrerende atomen energie overbrengen naar hun buren door botsingen. De nabijheid van deeltjes vergemakkelijkt de efficiënte energieoverdracht door dit mechanisme.
* gassen: Warmteoverdracht in gassen is voornamelijk door convectie , waar warmer, minder dicht gas stijgt en koeler, dichtere gaszinkmachines. Dit proces is minder efficiënt dan geleiding vanwege de grotere afstand tussen deeltjes en zwakkere interacties.
Samenvattend:
* vaste stoffen: Strakke verpakking en sterke interacties maken een efficiënte energieoverdracht mogelijk door geleiding.
* gassen: Brede afstand en zwakke interacties belemmeren energieoverdracht, waardoor ze slechte warmtegeleiders zijn.
Daarom zijn vaste stoffen over het algemeen betere warmtegeleiders dan gassen.
Hoofdlijnen
- Wat is een structuur in de wetenschap?
- Groot-Brittannië kondigt plan aan om handel in antiek ivoor te verbieden
- Hoe klimaatverandering planten onder druk zet en hun groei verandert
- Hoe onderzoekers een decennia-oud mysterie met betrekking tot celvolume hebben opgelost
- Wat is de rol van kloneringsvector in recombinante DNA -technologie?
- Studie biedt een model om te voorspellen hoe microbiomen op veranderingen kunnen reageren
- Micropropagatie van elite -soortenplanten?
- Hoe cellen worden verijdeld door een familielid van het herpesvirus in de wapenwedloop tussen virussen
- Wat is de stap van eiwitsynthese die voorkomt in de kern?
- Fluorescerend kristal mysterie opgelost
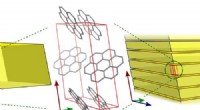
- Het conventionele begrip van antivries-eiwitten in twijfel trekken

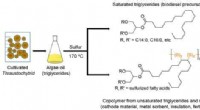
- Eenvoudige methode om hoogwaardige bioactieve stoffen te extraheren uit eencellige algenolie
- Belangrijke rol van singletzuurstof in synergetisch antimicrobieel mechanisme

- Continue en stabiele laserwerking dankzij goedkope perovskieten bij kamertemperatuur

 Welke van de volgende reacties demonstreert een synthesereactie A) Mg plus H2SO4 en gt MgSO4 H2 B) 2NaCl 2Na Cl2 C) C O2 CO2 D) Zn 2HCl ZnCl2 H2?
Welke van de volgende reacties demonstreert een synthesereactie A) Mg plus H2SO4 en gt MgSO4 H2 B) 2NaCl 2Na Cl2 C) C O2 CO2 D) Zn 2HCl ZnCl2 H2?  Waarom zou het wijzigen van de percentage samenstelling van een cent van 95 koper naar 97,5 zink het minder massief maken?
Waarom zou het wijzigen van de percentage samenstelling van een cent van 95 koper naar 97,5 zink het minder massief maken?  Wanneer licht van een ster de aarde bereikt, is het nog steeds?
Wanneer licht van een ster de aarde bereikt, is het nog steeds?  Wetenschappers onderzoeken het complexe patroon van omslagpunten in het huidige systeem van de Atlantische Oceaan
Wetenschappers onderzoeken het complexe patroon van omslagpunten in het huidige systeem van de Atlantische Oceaan  Wat zijn de zes factoren die fysieke verwering veroorzaken?
Wat zijn de zes factoren die fysieke verwering veroorzaken?  Magnetische geheugentoestanden worden exponentieel
Magnetische geheugentoestanden worden exponentieel Is de korst groter dan de kern?
Is de korst groter dan de kern?  Waarom voelen we de hitte van sterren niet?
Waarom voelen we de hitte van sterren niet?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


