
Wetenschap
Wat wordt geproduceerd wanneer niet -metalen oxide reageert met water?
* Niet -metalen oxiden worden vaak aangeduid als zure oxiden .
* Water is een neutraal molecuul, maar het kan in bepaalde reacties als basis werken.
Wanneer een niet -metalen oxide reageert met water, doneren de oxidemoleculen een proton (H+) aan de watermoleculen, waardoor hydroniumionen (H3O+) worden gevormd, wat het karakteristiek van een zuur is.
Hier zijn enkele voorbeelden:
* koolstofdioxide (CO2): CO2 + H2O -> H2CO3 (carbonzuur)
* zwaveldioxide (SO2): SO2 + H2O -> H2SO3 (zwavelzuur)
* stikstofdioxide (NO2): NO2 + H2O -> HNO3 + HNO2 (salpeterzuur en stikstofzuur)
Opmerking: De reactie van niet -metalen oxiden met water is vaak omkeerbaar, wat betekent dat het gevormde zuur onder bepaalde omstandigheden terug kan ontleden in het oxide en water.
 Wat zijn de drie dingen die Alfred Wegener gebruikte om zijn theorie over Pangea te bewijzen?
Wat zijn de drie dingen die Alfred Wegener gebruikte om zijn theorie over Pangea te bewijzen?  Wat is een soulutie die gelijk aantal waterstof- en hydroxylionen bevat?
Wat is een soulutie die gelijk aantal waterstof- en hydroxylionen bevat?  Wat is een niet-uniform mengsel?
Wat is een niet-uniform mengsel?  Hoeveel moleculen zitten er in een monster dimethylkwik van 7,85 g?
Hoeveel moleculen zitten er in een monster dimethylkwik van 7,85 g?  IBM kondigt op AI gebaseerd chemielab aan:RoboRXN
IBM kondigt op AI gebaseerd chemielab aan:RoboRXN
 Video:Sentinel-6 missie
Video:Sentinel-6 missie Lijst geërfde eigenschappen van een plant in het regenwoud?
Lijst geërfde eigenschappen van een plant in het regenwoud?  Als het regent, het giet - de effecten van regenwaterafvoer
Als het regent, het giet - de effecten van regenwaterafvoer Nationale parken zijn prachtig, maar bezuinigingen en ongelijkheid weerhouden velen ervan ervan te genieten
Nationale parken zijn prachtig, maar bezuinigingen en ongelijkheid weerhouden velen ervan ervan te genieten Ontdekking van metamorfe diamanten in het noordoosten van Queensland zou aanwijzingen kunnen geven over hoe Australië is ontstaan
Ontdekking van metamorfe diamanten in het noordoosten van Queensland zou aanwijzingen kunnen geven over hoe Australië is ontstaan
Hoofdlijnen
- Zijn celwandplanten of dieren?
- Welk type populatie zou de evolutie het snelst optreden?
- Sour Patch-volwassenen:1 op de 8 volwassenen houdt van extreme zuurheid, blijkt uit onderzoek
- Veerkracht van boomsoorten getest onder klimaatopwarming
- Hoe worden de gameten geproduceerd door Meiosis?
- Nieuwe inzichten in hoe KLF4 genexpressie beïnvloedt
- Hoe ondersteunt genetische variatie de natuurlijke selectie?
- Hoe komt stikstof uit levende organismen terug in de lucht?
- Het leven is mooi voor de imkers in Griekenland, maar hoe lang?
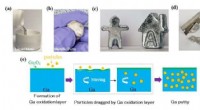
- Putty-achtige composieten van galliummetaal met potentieel voor toepassing in de echte wereld
- Verbrandingsgedrag van aromaten kan de sleutel zijn tot het verbeteren van de extractie van zware olie

- Het verrassingselement

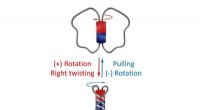
- Alles in orde:een omkeerbare moleculaire zweefmolen
- Analyse van magnetische materialen was nog nooit zo begrijpelijk

 Hoe watervlooien zich verdedigen tegen vleesetende planten
Hoe watervlooien zich verdedigen tegen vleesetende planten Wat is de wetenschappelijke methode in Renaissance?
Wat is de wetenschappelijke methode in Renaissance?  Steenkool en benzine zijn voorbeelden van.
Steenkool en benzine zijn voorbeelden van.  Het internet energiezuiniger maken door systemische optimalisatie
Het internet energiezuiniger maken door systemische optimalisatie Is er een vulkaan in Rocklin California?
Is er een vulkaan in Rocklin California?  Wat is olijfboomhabitat?
Wat is olijfboomhabitat?  Onderzoek wijst op ongekende en zorgwekkende stijging van de zeespiegel
Onderzoek wijst op ongekende en zorgwekkende stijging van de zeespiegel Nanoprobe maakt meting van eiwitdynamiek in levende cellen mogelijk
Nanoprobe maakt meting van eiwitdynamiek in levende cellen mogelijk
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

