
Wetenschap
Wat is de empirische formule van een stof die bestaat uit 5.687 g koper en 1.305 zuurstof?
1. Converteer grams naar mollen
* koper (cu): Verdeel de massa koper door zijn molaire massa (63,55 g/mol):
5.687 g Cu / 63,55 g / mol =0,0895 mol Cu
* zuurstof (O): Verdeel de zuurstofmassa door zijn molaire massa (16,00 g/mol):
1.305 g o / 16,00 g / mol =0,0816 mol O
2. Vind de molverhouding
* Verdeel het aantal mol van elk element door het kleinste aantal mol:
* Cu:0,0895 mol / 0,0816 mol =1,095 ≈ 1.1
* O:0,0816 mol / 0,0816 mol =1
3. Vereenvoudig de verhouding (indien nodig)
* Omdat we een verhouding hebben van ongeveer 1,1:1 voor Cu:O, vermenigvuldig beide zijden van de verhouding met 10 om hele getallen te krijgen:
* Cu:1,1 x 10 =11
* O:1 x 10 =10
4. Schrijf de empirische formule
* De empirische formule is cu₁₁o₁₀ .
Belangrijke opmerking: De empirische formule vertegenwoordigt de eenvoudigste verhouding van het hele nummer van atomen in een verbinding. Het is mogelijk dat de werkelijke moleculaire formule een veelvoud is van deze empirische formule.
 MLA-pipetten repareren
MLA-pipetten repareren  Is de uitsteeksel of vloeistof?
Is de uitsteeksel of vloeistof?  Waarom heeft fluor een kleinere atoomstraal dan zowel zuurstof als chloor?
Waarom heeft fluor een kleinere atoomstraal dan zowel zuurstof als chloor?  Ingenieur ontdekt waarom deeltjes zoals meel zich verspreiden over vloeistoffen
Ingenieur ontdekt waarom deeltjes zoals meel zich verspreiden over vloeistoffen  Nabijheid van actieve sites op maat van zeoliet voor efficiënte productie van pentaan-biobrandstoffen
Nabijheid van actieve sites op maat van zeoliet voor efficiënte productie van pentaan-biobrandstoffen
 Ring of Fire-vulkanen herinneren Azië aan seismisch gevaar
Ring of Fire-vulkanen herinneren Azië aan seismisch gevaar 180 landen sluiten VN-deal om de export van plastic afval te reguleren
180 landen sluiten VN-deal om de export van plastic afval te reguleren Wildvuur treft Brasilia National Park te midden van droogte
Wildvuur treft Brasilia National Park te midden van droogte NASA-NOAA-satelliet ziet systeem 91Ls elk in de westelijke golf van Mexico
NASA-NOAA-satelliet ziet systeem 91Ls elk in de westelijke golf van Mexico Planning voor toekomstige waterveiligheid in China
Planning voor toekomstige waterveiligheid in China
Hoofdlijnen
- Onderzoek bevestigt dat identiteitsverwisseling kan verklaren waarom haaien mensen bijten
- Leg uit hoe wordt het dubbele helixmodel van DNA gebouwd op onderzoek Rosalind Franklin?
- Wat zijn de niveaus van organisatie, van het minst tot het meest complexe -organ -tissue -systeem -cel -atoms en moleculen -cel?
- Het geheim van een langere levensduur? Genregulatie houdt een aanwijzing in
- Hebben menselijke embryo's en kanker dezelfde startlont?
- Oud menselijk DNA geeft aan waarom multiple sclerose tegenwoordig zoveel Noord-Europeanen treft
- Nieuw lid van NAS onthult hoe dieren goede microben selecteren en schadelijke microben afwijzen
- Hoe heeft technologie de manier veranderd waarop biologen levende wezens bestuderen?
- Wat is de wetenschappelijke naam van appelzaad?
- Het toevoegen van nog een laag metaalfluoride kan de prestaties van zonnecellen verbeteren

- Chemici ontdekken nieuwe reactiviteit van gespannen moleculen

- Onderzoekers bedenken nieuw proces om suikers uit hout te extraheren

- Water efficiënter omzetten in waterstof

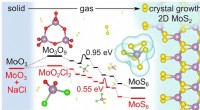
- Bestudeer details waarom 2D-vorming van molybdeendisulfide een snelheidsboost krijgt van zout
 Waarom waren de branden in de wijnlanden van Californië zo verwoestend?
Waarom waren de branden in de wijnlanden van Californië zo verwoestend?  Welke verbindingen elueert eerst in de niet -polaire GC -kolom?
Welke verbindingen elueert eerst in de niet -polaire GC -kolom?  Waar wordt graniet gedolven?
Waar wordt graniet gedolven?  Onderzoekers brengen het menselijk genoom in 4-D in kaart terwijl het vouwt
Onderzoekers brengen het menselijk genoom in 4-D in kaart terwijl het vouwt NASA ontwerpt vormveranderende robots voor de manen van Saturnus
NASA ontwerpt vormveranderende robots voor de manen van Saturnus Hoe de eerste ionisatie-energie van het waterstofatoom te berekenen met betrekking tot de Balmer-serie
Hoe de eerste ionisatie-energie van het waterstofatoom te berekenen met betrekking tot de Balmer-serie Dota 2 uitdagende bots worden moeilijk te verslaan nadat ze de coöperatieve modus hebben geleerd
Dota 2 uitdagende bots worden moeilijk te verslaan nadat ze de coöperatieve modus hebben geleerd Astronomen ontdekken een asteroïde van 2 km die dichter bij de zon draait dan Venus
Astronomen ontdekken een asteroïde van 2 km die dichter bij de zon draait dan Venus
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

