
Wetenschap
Wat is de trend in ionisatie -energie van Na Cl F?
Inzicht in ionisatie -energie
Ionisatie -energie is de minimale hoeveelheid energie die nodig is om een elektron uit een gasvormige atoom in de elektronische toestand van de grond te verwijderen.
Trend over een periode (van links naar rechts)
* Verhoogt: Ionisatie -energie neemt in het algemeen toe naarmate u van links naar rechts over een periode (rij) van de periodiek systeem gaat. Dit komt omdat:
* Nucleaire lading: Het aantal protonen in de kern neemt toe, wat leidt tot een sterkere aantrekkingskracht voor de elektronen.
* Effectieve nucleaire lading: De aantrekkingskracht van de kern voor de buitenste elektronen neemt toe, waardoor het moeilijker is om ze te verwijderen.
* Afscherming: Hoewel extra elektronen worden toegevoegd terwijl je over een periode beweegt, bevinden ze zich allemaal in hetzelfde belangrijkste energieniveau, dus afscherming van binnenste elektronen blijft relatief constant.
Trend een groep (van boven naar beneden)
* daalt: Ionisatie -energie neemt in het algemeen af als u een groep (kolom) van de periodieke tabel naar beneden beweegt. Dit komt omdat:
* Verhoogde afstand: Elektronen zijn verder weg van de kern in hogere energieniveaus en ervaren een zwakkere aantrekkingskracht.
* Verhoogde afscherming: Meer binnenste elektronenschillen zorgen voor meer afscherming, waardoor de aantrekkingskracht tussen de kern en de buitenste elektronen wordt verminderd.
De trend toepassen op NA, Cl en F
* F (fluor): Fluor bevindt zich rechtsboven in het periodiek systeem en heeft de hoogste ionisatie -energie van de drie. Het heeft een sterke nucleaire lading, een kleine atoomradius en minimale afscherming.
* CL (chloor): Chloor is onder fluor in dezelfde groep. De ionisatie -energie is lager omdat zijn valentie -elektronen verder van de kern zijn en meer afscherming ervaren.
* NA (natrium): Natrium zit in de eerste groep, wat betekent dat het slechts één valentie -elektron heeft. Dit elektron is relatief ver van de kern en ervaart aanzienlijke afscherming, waardoor het gemakkelijker te verwijderen is.
Samenvatting
De ionisatie -energietrend voor NA, CL en F volgt deze volgorde:
f> Cl> na
Dit betekent dat fluor de meeste energie vereist om een elektron te verwijderen, gevolgd door chloor, en natrium vereist de minste energie.
 Materiaal met hoge brekingsindex behoudt een hoge doorlaatbaarheid na uitgloeien bij 850 ° C
Materiaal met hoge brekingsindex behoudt een hoge doorlaatbaarheid na uitgloeien bij 850 ° C Pharma streeft naar een betere CBD
Pharma streeft naar een betere CBD Hernieuwbare oplosmiddelen afgeleid van lignine verlagen het afval bij de productie van biobrandstoffen
Hernieuwbare oplosmiddelen afgeleid van lignine verlagen het afval bij de productie van biobrandstoffen Wat is waar als u 2p- en 3p -orbitalen vergelijkt?
Wat is waar als u 2p- en 3p -orbitalen vergelijkt?  Welke methode kan worden gebruikt om kalium van zilver te scheiden?
Welke methode kan worden gebruikt om kalium van zilver te scheiden?
 Onderzoekers bouwen betere rotsmodellen
Onderzoekers bouwen betere rotsmodellen Onderzoekers onderzoeken hoe zoetwaterdiatomeeën in het licht blijven
Onderzoekers onderzoeken hoe zoetwaterdiatomeeën in het licht blijven  Jurassic wereld van vulkanen gevonden in centraal Australië
Jurassic wereld van vulkanen gevonden in centraal Australië De warmste winter in Moskou sinds het begin van de records:weerservice
De warmste winter in Moskou sinds het begin van de records:weerservice Hoe het onvoorspelbare te voorspellen in een veranderend klimaat?
Hoe het onvoorspelbare te voorspellen in een veranderend klimaat?
Hoofdlijnen
- Uitwerpselen van verstrikte Noord-Atlantische walvissen onthullen torenhoge stressniveaus
- Wat zijn twee hoofdtypen wetenschappelijk onderzoek?
- Wat is een analogie voor fagocytose?
- Verlegen knaagdieren zijn misschien beter in het overleven van uitroeiingen, maar geven ze deze eigenschappen door aan hun nakomelingen?
- Een evolutiepatroon waarin iets verschillende soorten evolueren van één gemeenschappelijke voorouder?
- Waar vindt aerobe en anerobe ademhaling plaats?
- Wat is de rol van mitochodria?
- Indringende vraag:Waarom overleefden zoogdieren het 'K/T-uitsterven'?
- Wat is een voorbeeld van culturele evolutie?
- Wetenschappers zetten aquacultuurafval om in nieuw biomateriaal voor weefselherstel

- Onderzoekers doen nieuwe ontdekking van mechanisme voor ladingopslag

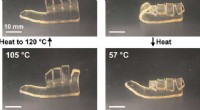
- Frontale polymerisatie afstemmen op diverse materiaaleigenschappen
- Nieuwe techniek kan voorheen niet-detecteerbare bacteriën aan het licht brengen op plaatsen waar ze niet gewenst zijn

- Hoge druk creëert nieuwe buren voor beryllium
 Wat is de stof die wordt opgelost?
Wat is de stof die wordt opgelost?  Blazar LBQS 1319+0039 gedetecteerd in harde röntgenstralen
Blazar LBQS 1319+0039 gedetecteerd in harde röntgenstralen Onderzoekers creëren DNA-draden die 100 keer gevoeliger zijn dan andere biosensoren
Onderzoekers creëren DNA-draden die 100 keer gevoeliger zijn dan andere biosensoren Welke vorm is het baanpatroon dat de aarde rond de zon neemt?
Welke vorm is het baanpatroon dat de aarde rond de zon neemt?  Waarom vereist een object met meer massa kracht om het te verplaatsen?
Waarom vereist een object met meer massa kracht om het te verplaatsen?  Synthesepaper onthult sterke en zwakke punten van milieubeloften van bedrijven
Synthesepaper onthult sterke en zwakke punten van milieubeloften van bedrijven Hoe tunnels werken
Hoe tunnels werken  Hoeveel is een knoop in termen van afstand en snelheid?
Hoeveel is een knoop in termen van afstand en snelheid?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

