
Wetenschap
Wat is het maximale aantal atomen dat een waterstof kan binden met een organische verbinding?
Hier is een uitsplitsing:
* Covalente binding: Waterstof kan een maximum van een vormen Covalente binding met een koolstofatoom in een organische verbinding. Dit komt omdat waterstof slechts één valentie -elektron heeft en het kan delen om een enkele binding te vormen.
* waterstofbinding: Waterstof kan deelnemen aan meerdere Waterstofbindingen met andere atomen in een organisch molecuul. Waterstofbinding is een zwakker type interactie, maar het speelt een cruciale rol in de structuur en eigenschappen van veel organische moleculen.
Voorbeeld: In een watermolecuul (H₂O) wordt elk waterstofatoom covalent gebonden aan het zuurstofatoom en kan het zuurstofatoom deelnemen aan twee waterstofbruggen met andere watermoleculen.
Daarom is het maximale aantal atomen waarmee een waterstofatoom kan "binden" in een organische verbinding, afhankelijk van het type binding dat u overweegt.
Als u geïnteresseerd bent in het aantal covalente bindingen , dan is het antwoord één . Als u overweegt waterstofbinding , dan is het antwoord complexer en afhankelijker van de specifieke organische verbinding.
 Is het waar dat een chemische reactie moleculen en verbindingen creëert?
Is het waar dat een chemische reactie moleculen en verbindingen creëert?  Hoe zonlicht elektronen activeert om stikstof te breken en ammoniak te vormen
Hoe zonlicht elektronen activeert om stikstof te breken en ammoniak te vormen Wat gebeurt er met alchemisten als ze hun werk niet doen?
Wat gebeurt er met alchemisten als ze hun werk niet doen?  Hoe worden de gassen die make -uplucht worden genoemd?
Hoe worden de gassen die make -uplucht worden genoemd?  Wat zijn alternatieven voor zoutzuur?
Wat zijn alternatieven voor zoutzuur?
 Een win-winsituatie voor bossen en kleinschalige melkveehouderij in Oost-Afrika
Een win-winsituatie voor bossen en kleinschalige melkveehouderij in Oost-Afrika Hoe landverontreiniging te voorkomen
Hoe landverontreiniging te voorkomen Onderzoekers onderzoeken hoe zoetwaterdiatomeeën in het licht blijven
Onderzoekers onderzoeken hoe zoetwaterdiatomeeën in het licht blijven  Welk type microscoop zou het beste zijn om een stuk beschimmeld brood te bekijken en waarom?
Welk type microscoop zou het beste zijn om een stuk beschimmeld brood te bekijken en waarom?  Nieuw rapport roept op tot onderzoek om beter te begrijpen, voorspel het lusstroomsysteem van de Golf van Mexico
Nieuw rapport roept op tot onderzoek om beter te begrijpen, voorspel het lusstroomsysteem van de Golf van Mexico
Hoofdlijnen
- Hoe zorgt heet water ervoor dat DNA vrijkomt in de celkernen?
- Wat moet u doen als u het defecte gen heeft?
- Aardworm Kenmerken
- Wat is wetenschappelijke variabele?
- Onderzoek wijst uit dat de meest nuttige habitat is voor de minste vliegenvanger
- Studenten zeggen dat ze een milieuvriendelijke manier hebben gevonden om Japanse kevers te vangen en te doden
- Hoe kunnen wetenschappers uitleg over gegevens ontwikkelen?
- Houden mannelijke vissen ze liever groot en kleurrijk?
- DNA-barcodes:zijn ze altijd nauwkeurig?
- Biologisch geïnspireerde kunstmatige spieren gemaakt van motoreiwitten
- Deponeren van ijzersoorten in ZSM-5 om cyclohexaan te oxideren tot cyclohexanon

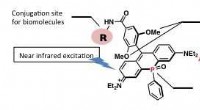
- Een nabij-infrarood fluorescerende kleurstof voor bio-imaging op lange termijn
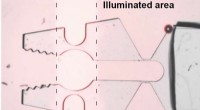
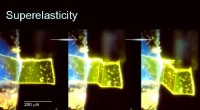
- Rood licht voor stress:een van kleur veranderend organisch kristal
- Flexibele vaste elektrolyten voor all-solid-state lithiumbatterijen

 Welke klasse verbindingen bevat alleen koolstofwaterstof en stikstof?
Welke klasse verbindingen bevat alleen koolstofwaterstof en stikstof?  Hack zet Latijns-Amerikaanse veiligheidsdiensten op scherp
Hack zet Latijns-Amerikaanse veiligheidsdiensten op scherp Hoe wordt een vulkanische nek gevormd?
Hoe wordt een vulkanische nek gevormd?  Overweegt u een smartapparaat te kopen? Stel uzelf deze vijf vragen om uw veiligheid te beschermen
Overweegt u een smartapparaat te kopen? Stel uzelf deze vijf vragen om uw veiligheid te beschermen Freud en Oedipus:doet een van beide er nog toe?
Freud en Oedipus:doet een van beide er nog toe?  De smalle opening aan het uiteinde van een raket?
De smalle opening aan het uiteinde van een raket?  Wetenschappers ontdekken hoe hoogenergetische elektronen magnetische velden versterken
Wetenschappers ontdekken hoe hoogenergetische elektronen magnetische velden versterken  Smartphones die worden gebruikt om migraties als gevolg van klimaatverandering te volgen
Smartphones die worden gebruikt om migraties als gevolg van klimaatverandering te volgen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

