
Wetenschap
Hoeveel valentie -elektronen heeft de boorgroep?
De boorgroep (groep 13) elementen hebben allemaal 3 valentie -elektronen .
Dit is waarom:
* valentie -elektronen zijn de elektronen in de buitenste schaal van een atoom, die betrokken zijn bij chemische binding.
* Groep 13 Elementen hebben allemaal hun buitenste elektronenconfiguratie als ns² np¹ .
Bijvoorbeeld:
* boron (b): 1S² 2S² 2P¹ (3 valentie -elektronen)
* aluminium (AL): 1S² 2S² 2P⁶ 3S² 3P¹ (3 valentie -elektronen)
* Gallium (GA): 1S² 2S² 2P⁶ 3S² 3P⁶ 4S² 3D¹⁰ 4P¹ (3 valentie -elektronen)
* indium (in): 1S² 2S² 2P⁶ 3S² 3P⁶ 4S² 3D¹⁰ 4P⁶ 5S² 4D¹⁰ 5P¹ (3 valentie -elektronen)
* thallium (tl): 1S² 2S² 2P⁶ 3S² 3P⁶ 4S² 3D¹⁰ 4P⁶ 5S² 4d¹⁰ 5p⁶ 6S² 4F¹⁴ 5d¹⁰ 6p¹ (3 valentie -elektronen)
Hoofdlijnen
- Wat is waar aan de genenpool en genetische diversiteit?
- Waarom wordt Euglena geclassificeerd als een protoktist en geen dier of plant?
- Wat betekent niche in de wetenschap?
- Walviskarkas opgegraven van Australisch strand vanwege angst voor haaien
- Hoe bacteriën hypothiocyaniet onschadelijk maken, een antimicrobieel wapen van het aangeboren immuunsysteem
- Wat zijn de twee belangrijkste componenten van celmembranen?
- Onderzoekers concentreren zich op de manier waarop bacteriën voedselvergiftiging veroorzaken
- Laten tenen schimmel groeien. Omdat de teen van Piper Rockelles er beschimmeld uitziet?
- Wat reguleert de eiwitproductie in de kern?
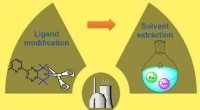
- Molecuulmodificatie kan de opwerking van verbruikte splijtstof verbeteren
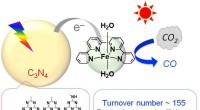
- CO2 verminderen met gemeenschappelijke elementen en zonlicht
- Polymeerbeweging:sleutel tot coatings van de volgende generatie

- De universele taal van hormonen

- Onderzoekers hebben bewezen dat ozon effectief is bij het desinfecteren van coronavirus

 Waarom is het chemische verandering wanneer een zilveren vork langzaam in de lucht aftast?
Waarom is het chemische verandering wanneer een zilveren vork langzaam in de lucht aftast?  Titaandioxide nanoreactor
Titaandioxide nanoreactor Fluor versnelt de groei van tweedimensionale materialen
Fluor versnelt de groei van tweedimensionale materialen Welk waterlichaam ligt op de 0 lijn breedtegraad en 140 West -lengtegraad?
Welk waterlichaam ligt op de 0 lijn breedtegraad en 140 West -lengtegraad?  Het gepersonaliseerde algoritme voor de afspeellijst voor DJ-muziek stemt nummers af op de veranderende stemming van luisteraars
Het gepersonaliseerde algoritme voor de afspeellijst voor DJ-muziek stemt nummers af op de veranderende stemming van luisteraars Wat verontrust atleten die in Rio aankomen? Geen 'Pokemon Go'
Wat verontrust atleten die in Rio aankomen? Geen 'Pokemon Go'  Video:De koolstofcyclus
Video:De koolstofcyclus GPS-begeleiding kan voor de gek gehouden worden, dus onderzoekers klauteren op zoek naar back-uptechnologieën
GPS-begeleiding kan voor de gek gehouden worden, dus onderzoekers klauteren op zoek naar back-uptechnologieën
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


