
Wetenschap
Wat is een gigantisch moleculair kristal?
Hier is een uitsplitsing van belangrijke functies:
* Grote moleculen: De fundamentele eenheden van het kristal zijn moleculen, die worden gevormd door covalente bindingen in het molecuul.
* Covalente binding: Sterke covalente bindingen verbinden de atomen in het molecuul en de moleculen worden bij elkaar gehouden in een continu netwerk door verdere covalente bindingen.
* Uitgebreide structuur: Er zijn geen verschillende moleculaire eenheden. In plaats daarvan vormen de covalente bindingen een continue, uitgebreide structuur, waardoor het hele kristal in wezen één gigantisch molecuul is.
* Hoog smelten- en kookpunten: Vanwege de sterke covalente bindingen hebben gigantische moleculaire kristallen hoge smelt- en kookpunten. Ze vereisen aanzienlijke energie om de bindingen te verbreken en de moleculen te scheiden.
Voorbeelden:
* diamant: Koolstofatomen zijn verbonden in een tetraëdrische opstelling door sterke covalente bindingen. Dit creëert een gigantisch moleculair kristal met uitzonderlijke hardheid en hoog smeltpunt.
* siliciumdioxide (SiO2): De basiseenheid is de SiO4-tetraëder, die een driedimensionaal netwerk vormt met sterke covalente bindingen. Dit geeft silica zijn hoge smeltpunt en brosse aard.
* grafiet: Koolstofatomen vormen lagen bij elkaar gehouden door zwakkere van der Waals -krachten, terwijl binnen de lagen sterke covalente bindingen een gigantische moleculaire structuur creëren. Dit verklaart de gelaagde structuur en verschillende eigenschappen van grafiet in vergelijking met diamant.
Belangrijke verschillen van ionische en metalen kristallen:
* ionische kristallen: Samen gehouden door elektrostatische krachten tussen ionen.
* metalen kristallen: Samen gehouden door delokaliseerde elektronen in een "zee" van elektronen.
Gigantische moleculaire kristallen worden daarentegen uitsluitend bij elkaar gehouden door een continu netwerk van covalent bindingen .
Inzicht in de eigenschappen van gigantische moleculaire kristallen is essentieel in velden zoals Materials Science, waar hun unieke kenmerken, zoals hoge hardheid en thermische stabiliteit, ze waardevol maken voor toepassingen zoals halfgeleiders en industriële hulpmiddelen.
 Nieuwe synthesestrategie versnelt identificatie van eenvoudigere versies van een natuurlijk product
Nieuwe synthesestrategie versnelt identificatie van eenvoudigere versies van een natuurlijk product Het leveren van genetisch materiaal met MOF's voor nieuwe therapieën
Het leveren van genetisch materiaal met MOF's voor nieuwe therapieën Is lithium bij kamertemperatuur vast, vloeibaar of gasvormig?
Is lithium bij kamertemperatuur vast, vloeibaar of gasvormig?  Hoe folin-ciocalteu werkt in de totale methode voor fenolische inhoud?
Hoe folin-ciocalteu werkt in de totale methode voor fenolische inhoud?  Twee atomen zijn isotopen van hetzelfde element. Wat zou voor deze twee atomen moeten zijn?
Twee atomen zijn isotopen van hetzelfde element. Wat zou voor deze twee atomen moeten zijn?
 Hoe een temperatuurstijging van 1,5 graden Celsius aanzienlijke veranderingen bij kustsoorten kan veroorzaken
Hoe een temperatuurstijging van 1,5 graden Celsius aanzienlijke veranderingen bij kustsoorten kan veroorzaken  Afbeelding:Amazonebranden blijven Zuid-Amerika in rook hullen
Afbeelding:Amazonebranden blijven Zuid-Amerika in rook hullen Studie onderzoekt hoe media over de hele wereld nieuws over klimaatverandering framen
Studie onderzoekt hoe media over de hele wereld nieuws over klimaatverandering framen Scholen in New Delhi gesloten vanwege giftige smog
Scholen in New Delhi gesloten vanwege giftige smog Wat is de basis van alle levende wezens?
Wat is de basis van alle levende wezens?
Hoofdlijnen
- Hoe verzamel en analyseer je bacteriën?
- Welke celstructuur wordt gemaakt in G1?
- Leg uit waarom stikstof belangrijk is voor organismen?
- Gymnospermen: definitie, levenscyclus, typen en voorbeelden
- Wat is een voorbeeld van bioremediatie?
- Wat is een tyroid?
- geproduceerd door het lichaam om u te helpen beschermen tegen ziekten?
- De wetenschap zegt:waarom wetenschappers planten- en dierengenomen waarderen
- Wat zijn de drie soorten klonen in eenvoudige vorm?
- Vechten tegen een machtig onkruid

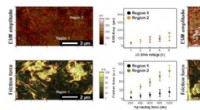
- Visualisatie van functionele componenten om optimale composietelektroden te karakteriseren
- Wetenschappers identificeren nieuwe katalysatoren voor efficiëntere watersplitsing

- Wetenschappers testen nieuw materiaal voor neurocomputers

- Nieuwe studies van oud beton zouden ons kunnen leren te doen zoals de Romeinen deden

 Wat is de lengte van Apollo11 -ruimtevaartuigen?
Wat is de lengte van Apollo11 -ruimtevaartuigen?  Hoeveel Fahrenheit is 200 C?
Hoeveel Fahrenheit is 200 C?  Hoe kunnen we de curve van het biodiversiteitsverlies ombuigen? Nieuw analytisch raamwerk biedt antwoorden
Hoe kunnen we de curve van het biodiversiteitsverlies ombuigen? Nieuw analytisch raamwerk biedt antwoorden  Impliceert de nieuwe slogan van Google een verschuiving naar zakelijke apps?
Impliceert de nieuwe slogan van Google een verschuiving naar zakelijke apps?  Google bouwt gebarenbediening in nieuwe Pixel-telefoon
Google bouwt gebarenbediening in nieuwe Pixel-telefoon Waarom is kopercarbonaat gevaarlijk?
Waarom is kopercarbonaat gevaarlijk?  Wat is 0,00075 in wetenschappelijke notatie?
Wat is 0,00075 in wetenschappelijke notatie?  Onderzoekers ontwikkelen eerste hittekaart voor individuele rode bloedcellen
Onderzoekers ontwikkelen eerste hittekaart voor individuele rode bloedcellen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

