
Wetenschap
Wat is de massa van 150 liter stikstofgas (N2)?
1. Ideale gaswet:
* De ideale gaswet is een goede benadering voor gassen onder normale omstandigheden. Het staat: pv =nrt
* P =druk (in pascals)
* V =volume (in kubieke meter)
* n =aantal mol
* R =ideale gasconstante (8.314 J/mol · k)
* T =temperatuur (in kelvin)
2. Converteren eenheden:
* Volume: 150 liter =0,15 kubieke meter (1 liter =0,001 kubieke meter)
* Ga uit van standaardtemperatuur en druk (STP):
* Temperatuur (t) =273,15 K (0 ° C)
* Druk (P) =101325 PA (1 atm)
3. Oplossen voor mol (n):
* Herschik de ideale gaswetvergelijking: n =(pv) / (rt)
* Vervang de waarden:n =(101325 PA * 0,15 m³) / (8.314 j / mol · k * 273.15 k)
* Bereken:n ≈ 6,68 mol stikstofgas
4. Bereken massa:
* Molaire massa van N₂: 28.01 g/mol
* massa =mol * molaire massa: Massa ≈ 6,68 mol * 28.01 g/mol ≈ 187.05 g
Daarom is de massa van 150 liter stikstofgas bij STP ongeveer 187,05 gram.
Hoofdlijnen
- Wetenschappers begrijpen hoe de E. coli-kloon wereldwijd verspreid is geraakt
- Wat zijn de special in celmembraan waarmee materialen zoals water en suiker door maakten worden doorgemaakt?
- Wat gitaarvissen en vliegtuigvleugels gemeen hebben
- Waar is selectief permeabele membraan gevonden in planten?
- Zeldzame zangvogel heeft misschien nooit bestaan
- Menselijk genoom bevat hoeveel?
- Hoe cellen op de juiste manier reageren in barre omgevingen als gevolg van de opwarming van de aarde
- Optimale groepsgroottes verschillen per geslacht bij coöperatieve dieren
- Hoe maak je een 3D-model van de dikke darm
- De wetenschap achter ingelegde elektrolyten in batterijen
- Gouden microjuwelen uit de 3D-printer

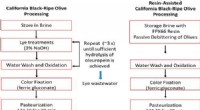
- Een groenere manier om de bitterheid uit olijven te halen
- Wetenschappers testen met succes nieuwe, veiligere titaniumplaat voor herstel van botweefsel

- Monitoring van de corrosie van bioresorbeerbaar magnesium

 Hoe kun je zien of wasmiddel biologisch is of niet?
Hoe kun je zien of wasmiddel biologisch is of niet?  SwRI-spectrograaf om enkele van de mysteries van de zon te helpen beantwoorden
SwRI-spectrograaf om enkele van de mysteries van de zon te helpen beantwoorden Kunnen er manen zijn die asteroïden uit de asteroïde riem kunnen worden getrokken?
Kunnen er manen zijn die asteroïden uit de asteroïde riem kunnen worden getrokken?  Waar de oceaan de lucht ontmoet - nieuwe NASA-radar krijgt een try-out
Waar de oceaan de lucht ontmoet - nieuwe NASA-radar krijgt een try-out De waarde van samenwerking voor duurzame ontwikkeling in grensoverschrijdende stroomgebieden
De waarde van samenwerking voor duurzame ontwikkeling in grensoverschrijdende stroomgebieden Wetenschappers vinden een nieuw mechanisme voor de stabilisatie van skyrmionen
Wetenschappers vinden een nieuw mechanisme voor de stabilisatie van skyrmionen Wat is een genosfeer?
Wat is een genosfeer?  Een studie legt de complexiteit uit van de vestiging van Azië door Homo sapiens
Een studie legt de complexiteit uit van de vestiging van Azië door Homo sapiens
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


