
Wetenschap
Hoe is oplosbaarheid gerelateerd aan temperatuur?
Algemene trends:
* vaste stoffen: Voor de meeste solide opgeloste stoffen neemt de oplosbaarheid toe met toenemende temperatuur . Dit komt omdat verhoogde thermische energie de opgeloste deeltjes in staat stelt de aantrekkelijke krachten te overwinnen die ze in de vaste toestand houden, waardoor ze kunnen loskomen en oplossen.
* gassen: Voor de meeste gasvormige opgeloste stoffen neemt de oplosbaarheid van af met toenemende temperatuur . Dit komt omdat bij hogere temperaturen gasmoleculen meer kinetische energie hebben en meer kans hebben om uit de vloeibare oplossing naar de omringende atmosfeer te ontsnappen.
Uitzonderingen:
* Sommige vaste stoffen vertonen een afname van de oplosbaarheid met toenemende temperatuur. Dit gebeurt wanneer het oplossingsproces exotherme is (warmte vrijgeeft). In deze gevallen verschuift de toenemende temperatuur het evenwicht naar de vorming van niet -opgeloste vaste stof.
* Sommige gassen vertonen een toename van de oplosbaarheid met toenemende temperatuur. Dit gebeurt wanneer het oplossingsproces endotherm is (absorbeert warmte). De toename van de temperatuur is voorstander van het oplossingsproces, wat leidt tot een hogere oplosbaarheid.
factoren die de relatie beïnvloeden:
* Aard van de opgeloste stof en oplosmiddel: De specifieke eigenschappen van de opgeloste stof en oplosmiddel spelen een belangrijke rol bij het bepalen van het oplosbaarheidsgedrag.
* Druk: Voor gassen kan druk de oplosbaarheid aanzienlijk beïnvloeden. Hogere druk leidt tot hogere oplosbaarheid.
* polariteit: Opgeloste stoffen lost de neiging om beter op te lossen in oplosmiddelen met vergelijkbare polariteiten.
Inzicht in de relatie:
Om de relatie tussen oplosbaarheid en temperatuur te begrijpen, is het belangrijk om de enthalpieverandering (ΔH) van oplossing te overwegen .
* exotherme oplossing (ΔH <0): Het oplossingsproces geeft warmte vrij. Toenemende temperatuur verschuift het evenwicht naar de vorming van niet -opgeloste vaste stof, wat resulteert in een afname van de oplosbaarheid.
* Endothermische oplossing (ΔH> 0): Het oplossingsproces absorbeert warmte. Toenemende temperatuur verschuift het evenwicht naar de vorming van opgeloste opgeloste stof, wat resulteert in een toename van de oplosbaarheid.
Samenvattend:
Hoewel er algemene trends zijn, kan de relatie tussen oplosbaarheid en temperatuur complex zijn en variëren afhankelijk van de specifieke stof die wordt opgelost. Inzicht in de enthalpieverandering van ontbinding kan helpen de richting van verandering in oplosbaarheid met temperatuur te voorspellen.
 First Nation-knowhow om onze landschappen te helpen redden
First Nation-knowhow om onze landschappen te helpen redden  Hoe heet de wetenschap die de hele aarde bestudeert?
Hoe heet de wetenschap die de hele aarde bestudeert?  Hitte is een serieuze bedreiging voor melkkoeien - vonden innovatieve manieren om ze koel te houden
Hitte is een serieuze bedreiging voor melkkoeien - vonden innovatieve manieren om ze koel te houden Studie onthult de complexiteit van microplasticvervuiling
Studie onthult de complexiteit van microplasticvervuiling Nutriëntenrecyclerende microben kunnen de hitte voelen
Nutriëntenrecyclerende microben kunnen de hitte voelen
Hoofdlijnen
- Vrouwelijke hagedis draait de tafel om:waarom overdreven kleuring haar een goede partner maakt
- Hoe bacteriën eiwitten exploiteren om potentieel dodelijke infecties te veroorzaken
- Simulaties laten zien hoe bèta-amyloïde neurale cellen kan doden
- Wormetende muizen laten zien hoe evolutie werkt op eilanden
- Welk van de drie regio's bevat het oss van de regio's?
- Hoe zou een dieren zijn extra opgeslagen suiker vrijgeven?
- Reguleren de longen de pH-balans?
- Welke klier initieert de groei en andere fysieke veranderingen van de adolescentie?
- Waarom is stamcelbehandeling een wetenschappelijke controverse?
- Een nieuwe strategie om blauw licht te creëren uit een veelbelovend materiaal
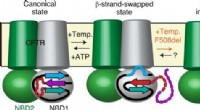
- Uiterlijk van cystische fibrose op moleculaire schaal
- Ultrasone techniek onthult de identiteit van grafiet

- Kunstmatige fotosynthese kan nutteloos kooldioxide omzetten in mierenzuur dat in de industrie wordt gebruikt

- Tijdmachine biedt nieuwe aanpak voor het testen van geneesmiddelen voor alvleesklierkanker

 Onzekerheid thuishoren in STEM-cursussen kan van invloed zijn op cijfers
Onzekerheid thuishoren in STEM-cursussen kan van invloed zijn op cijfers Hoe een biologisch diagram te tekenen
Hoe een biologisch diagram te tekenen  Ierland recupereert 14 miljard euro aan achterstallige Apple belastingen
Ierland recupereert 14 miljard euro aan achterstallige Apple belastingen Wat is de massa van 6,0 mol natriumnitraat (NaNO3)?
Wat is de massa van 6,0 mol natriumnitraat (NaNO3)?  Toen Mendeleyev de lay-out veranderde, waren er gapshows. Hebben grappen wetenschappers geholpen bij het zoeken naar onontdekte elementen?
Toen Mendeleyev de lay-out veranderde, waren er gapshows. Hebben grappen wetenschappers geholpen bij het zoeken naar onontdekte elementen?  Microsofts nieuwe Xbox-controller maakt gamers met een handicap voor de rechter
Microsofts nieuwe Xbox-controller maakt gamers met een handicap voor de rechter Post-Sovjet-Unie geluksvertraging tussen Oost- en West-Europa uitgelegd
Post-Sovjet-Unie geluksvertraging tussen Oost- en West-Europa uitgelegd Waarom is het minder waarschijnlijk dat rijke consumenten luxeartikelen kopen tijdens een recessie?
Waarom is het minder waarschijnlijk dat rijke consumenten luxeartikelen kopen tijdens een recessie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

