
Wetenschap
Is een zeer brandbare stof ook reactieve substantie?
brandbaarheid Verwijst naar het gemak waarmee een stof ontsteekt en brandt. Dit wordt grotendeels bepaald door zijn:
* Flash Point: De laagste temperatuur waarbij een stof voldoende damp afgeeft om te ontsteken.
* ontstekingstemperatuur: De minimale temperatuur die nodig is om verbranding te initiëren zonder een externe ontstekingsbron.
reactiviteit Beschrijft hoe gemakkelijk een stof chemische verandering ondergaat, vooral in relatie tot andere stoffen. Dit kan inhouden:
* oxidatie: Reactie met zuurstof, die warmte kan afgeven en explosief kan zijn.
* Redox -reacties: Reacties met betrekking tot de overdracht van elektronen.
* Ontleding: Afbreken in eenvoudigere stoffen.
Hier is de verbinding:
* Veel zeer brandbare stoffen zijn reactief: Ze reageren gemakkelijk met zuurstof, vaak op een snelle en exotherme manier, wat verbranding veroorzaakt. Dit is de reden waarom ontvlambare vloeistoffen zoals benzine zeer reactief zijn met zuurstof.
* Niet alle reactieve stoffen zijn zeer brandbaar: Sommige stoffen kunnen gemakkelijk reageren zonder brand te betrekken. Natrium reageert bijvoorbeeld krachtig met water, produceert warmte- en waterstofgas, maar deze reactie wordt niet beschouwd als verbranding.
Voorbeelden:
* zeer brandbaar en reactief: Diethylether, benzine, methaan
* zeer brandbaar, maar niet noodzakelijkerwijs zeer reactief: Hout, papier (verbranding is een complexe reactie met zuurstof, maar niet noodzakelijkerwijs een "reactieve" stof in chemische zin)
* reactief, maar niet zeer brandbaar: Natriummetaal (reageert gewelddadig met water, maar brandt niet)
Samenvattend:
VERBRANDBAARHEID EN REACTIVITEIT zijn gerelateerde concepten maar niet synoniem. Hoewel veel brandbare stoffen reactief zijn, zijn niet alle reactieve stoffen brandbaar.
 Onderzoekers produceren allereerste video's van chemische synthese met atomaire resolutie
Onderzoekers produceren allereerste video's van chemische synthese met atomaire resolutie Realtime atomaire beweging volgen tussen kristalkorrels in metalen
Realtime atomaire beweging volgen tussen kristalkorrels in metalen Zelfassemblage van polypeptiden geleid door toevoeging van co-oplosmiddelen
Zelfassemblage van polypeptiden geleid door toevoeging van co-oplosmiddelen Nieuwe techniek volgt individuele eiwitbeweging op levende cellen
Nieuwe techniek volgt individuele eiwitbeweging op levende cellen De zoektocht naar medicijnen tegen obesitas richt zich op de complexe chemie van honger
De zoektocht naar medicijnen tegen obesitas richt zich op de complexe chemie van honger
 Wat zijn de drie grote afdelingen van de biologie?
Wat zijn de drie grote afdelingen van de biologie?  De plasticcrisis heeft diepe wortels in het bedrijfsleven:om onze planeet te beschermen, moeten ze worden blootgesteld
De plasticcrisis heeft diepe wortels in het bedrijfsleven:om onze planeet te beschermen, moeten ze worden blootgesteld Een nieuwe aanpak voor 24/7 monitoring van de luchtkwaliteit met behulp van camera's
Een nieuwe aanpak voor 24/7 monitoring van de luchtkwaliteit met behulp van camera's  Hoe verspreiden vogels zaden?
Hoe verspreiden vogels zaden?  Hoe beïnvloedt luchtmassa het klimaat?
Hoe beïnvloedt luchtmassa het klimaat?
Een luchtmassa is een grote eenheid van de lagere atmosfeer die wordt gedefinieerd door gemeenschappelijke fysieke kenmerken, zoals temperatuur en vochtigheid, op elke gegeven hoogte en een die onopvallend en
Hoofdlijnen
- Wat maakt een succesvolle samenleving? Sociale wetenschappers vinden de gezondheidszorg slechts een stukje van de puzzel
- Nieuwe studie vergroot het begrip van hoe antibioticaresistentie ontstaat
- Een nieuw begrip van hoe cellen zichzelf verdedigen tegen bacteriële porievormende toxines
- Hoe evolutie de magnetische sensor bij vogels heeft geoptimaliseerd
- Bedreigen otters amfibieënpopulaties?
- Ontdekken hoe T-cellen het spike-eiwit van het SARS-COV-2-virus herkennen
- Welk product is niet gerelateerd aan geneeskunde?
- Een viraal verhulapparaat:Biologen laten zien hoe het menselijke cytomegalovirus zich verbergt voor het immuunsysteem
- Hoe wordt het proces genoemd waarin culturen meer en lijken op elkaar worden?
- Een zilveren randje voor extreme elektronica

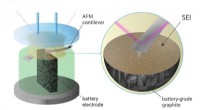
- Wetenschappers krijgen een voorproefje van een belangrijk proces in de levensduur van de batterij
- Nieuwe analytische techniek helpt onderzoekers subtiele verschillen in subcellulaire chemie op te sporen

- Natuurkundigen leggen uit hoe grote bolvormige virussen worden gevormd

- Het in kaart brengen van de driedimensionale structuur van katalytische centra helpt bij het ontwerpen van nieuwe en verbeterde katalysatoren
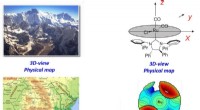
 Welke stad is 39 graden North Latitude en 90 West Loogte?
Welke stad is 39 graden North Latitude en 90 West Loogte?  Licht uit:de oxidatie van de omgevingslucht van monolaag wolfraamdisulfide naar bed brengen
Licht uit:de oxidatie van de omgevingslucht van monolaag wolfraamdisulfide naar bed brengen Hoogste gehalte aan microplastics in weekdieren, nieuwe studie zegt
Hoogste gehalte aan microplastics in weekdieren, nieuwe studie zegt Hoe snel kan een mens fietsen? Met aerodynamische hulp, de 300km per uur barrière lijkt binnen handbereik
Hoe snel kan een mens fietsen? Met aerodynamische hulp, de 300km per uur barrière lijkt binnen handbereik Snelle bodemtest is bedoeld om stikstofbehoefte te bepalen
Snelle bodemtest is bedoeld om stikstofbehoefte te bepalen Satelliet vangt nachtelijke opname van grote orkaan Teddy
Satelliet vangt nachtelijke opname van grote orkaan Teddy Onderzoekers ontwikkelen spuit-injecteerbare, zelfuitbreidbare en ultraaanpasbare magnetische nanosheets
Onderzoekers ontwikkelen spuit-injecteerbare, zelfuitbreidbare en ultraaanpasbare magnetische nanosheets Wetenschappers doen magnetische nieuwe ontdekking van grafeen
Wetenschappers doen magnetische nieuwe ontdekking van grafeen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

