
Wetenschap
Waarom werd koolstof gekozen als basis Amu Thay had een ander element kunnen gebruiken?
* overvloed: Koolstof is een relatief overvloedig element in het universum en op aarde. Dit maakt het gemakkelijker om voor wetenschappelijke doeleinden te verkrijgen en mee te werken.
* veelzijdige chemie: Koolstof vormt een breed scala aan verbindingen, waardoor het cruciaal is voor vele gebieden van chemie. Het kiezen van koolstof als basiseenheid helpt de berekeningen en relaties binnen die velden te vereenvoudigen.
* Handige massa: Carbon-12, de meest voorkomende isotoop van koolstof, heeft een atoommassa bijna 12. Dit maakte het handig om 1 AMU te definiëren als 1/12 de massa van een koolstof-12-atoom.
Historische context:
* Aanvankelijk werd waterstof gebruikt als standaard voor atomaire massa. Waterstof is echter zeer reactief en moeilijk om nauwkeurig mee te werken.
* Zuurstof werd later gekozen als standaard, maar verschillende waarden voor zijn atoommassa werden door verschillende onderzoekers gebruikt, wat leidde tot verwarring.
* In 1961 heeft de International Union of Pure and Applied Chemistry (IUPAC) Carbon-12 aangenomen als de standaard voor atomaire massa, die een uniform en nauwkeuriger systeem opleverde.
Samenvattend werd koolstof gekozen als basis voor AMU vanwege de overvloed, chemische veelzijdigheid en handige atoommassa. Deze keuze gestroomlijnde wetenschappelijke berekeningen en heeft een universeel geaccepteerde standaard vastgesteld.
 Bio-sensing contactlens kan op een dag bloedglucose meten, andere lichaamsfuncties
Bio-sensing contactlens kan op een dag bloedglucose meten, andere lichaamsfuncties Onderzoekers beoordelen de state-of-the-art text mining-technologieën voor chemie
Onderzoekers beoordelen de state-of-the-art text mining-technologieën voor chemie Nieuw ontworpen liganden voor een katalytische reactie om medicijnen en nuttige verbindingen te synthetiseren
Nieuw ontworpen liganden voor een katalytische reactie om medicijnen en nuttige verbindingen te synthetiseren Nieuwe enzymontdekking kan geneesmiddelen tegen kanker helpen verbeteren, diabetes en obesitas
Nieuwe enzymontdekking kan geneesmiddelen tegen kanker helpen verbeteren, diabetes en obesitas Wetenschappers ontdekken de sleutel tot een potentiële natuurlijke potentie voor kankerbehandelingen
Wetenschappers ontdekken de sleutel tot een potentiële natuurlijke potentie voor kankerbehandelingen
 NASA vindt windschering die de tropische cycloon Uesi . treft
NASA vindt windschering die de tropische cycloon Uesi . treft Prins Charles waarschuwt voor plastic op het menu bij vis ter wereld
Prins Charles waarschuwt voor plastic op het menu bij vis ter wereld Nieuwe karteringstechnieken stellen onderzoekers in staat om het effect van gletsjerstroom op infrastructuur beter te meten, omgeving
Nieuwe karteringstechnieken stellen onderzoekers in staat om het effect van gletsjerstroom op infrastructuur beter te meten, omgeving Waarom zaaien we zaden rechtstreeks in de grond?
Waarom zaaien we zaden rechtstreeks in de grond?  Gezondheidswaarschuwingen en snelheidslimieten terwijl Europa in een hittegolf raast
Gezondheidswaarschuwingen en snelheidslimieten terwijl Europa in een hittegolf raast
Hoofdlijnen
- Nieuw onderzoek wijst uit waarom sommige microbiële genen meer promiscue zijn dan andere
- Hoe eiwitten in gist communiceren om partners te vinden
- Wat heeft er naast een celmembraan?
- Het Tea Tree-genoom bevat aanwijzingen over hoe één blad zoveel smaken produceert
- Wat zijn de twee processen die zich voordoen terwijl het organisme leeft, maar ophouden wanneer het dood is?
- Wat zijn de twee manieren waarop schimmels sporen produceren?
- Waar bevinden zich de mitochondriën in de dierlijke cel?
- Dissectie van één molecuul van ontwikkelingsgencontrole
- Modellen tonen aan dat koralen beter bestand zijn tegen de opwarming van de oceaan als ze ruilen voor hittebestendige algenvariëteiten
- Wetenschappers tonen aan dat een veelbelovende vaste elektrolyt hydrofoob is
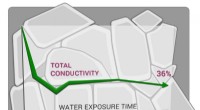
- Nieuw voedsel invriesconcept verbetert kwaliteit, verhoogt de veiligheid, vermindert energieverbruik

- Shagene Een synthese geperfectioneerd voor de behandeling van leishmaniasis
- Vloeistoffen filteren met vloeistoffen bespaart elektriciteit

- Ingenieurs veranderen plastic isolator in warmtegeleider

 Is een vermogen om een fysieke eigenschap te verbranden?
Is een vermogen om een fysieke eigenschap te verbranden?  Een nieuw mechanisme verbetert de efficiëntie van antibacteriële oppervlakken
Een nieuw mechanisme verbetert de efficiëntie van antibacteriële oppervlakken Wat is het oxidatiegetal van S in H2S?
Wat is het oxidatiegetal van S in H2S?  In een formule zonder haakjes is subscript van toepassing?
In een formule zonder haakjes is subscript van toepassing?  Nieuwe geleiders met een hoog protonengehalte met inherent zuurstofarme lagen openen een duurzame toekomst
Nieuwe geleiders met een hoog protonengehalte met inherent zuurstofarme lagen openen een duurzame toekomst Hoe wordt een bij een bijenkoningin?
Hoe wordt een bij een bijenkoningin?  Experimenten om het wetenschappelijk begrip te vervolledigen van hoe verminderde zwaartekracht het koken en condensatie beïnvloedt
Experimenten om het wetenschappelijk begrip te vervolledigen van hoe verminderde zwaartekracht het koken en condensatie beïnvloedt  SAS pilootstaking strandt 72, 000 passagiers
SAS pilootstaking strandt 72, 000 passagiers
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

