
Wetenschap
Is een atoom met atoomnummer van 1 stabiel?
Dit is waarom:
* waterstof bestaat als een diatomisch molecuul (H2) . Twee waterstofatomen delen hun elektronen om een stabiele covalente binding te vormen, waardoor het molecuul dat we kennen als waterstofgas creëert. Deze binding voldoet aan de octetregel en maakt het molecuul stabieler dan individuele waterstofatomen.
* isotopen: Hoewel waterstof het meest voorkomende element in het universum is, bestaat het in verschillende isotopen:
* protium (1H): Dit is de meest voorkomende isotoop, bestaande uit één proton en één elektron.
* deuterium (2H): Bevat één proton, één neutron en één elektron. Het is stabiel.
* tritium (3H): Bevat één proton, twee neutronen en één elektron. Het is radioactief en vervalt in de loop van de tijd.
Hoewel het atoomnummer 1 waterstof vertegenwoordigt, is het daarom niet stabiel in zijn pure vorm. Het moet binden aan een ander waterstofatoom om een stabiel diatomee -molecuul te vormen.
 Waarom is gedestilleerd water niet geschikt om te drinken, ook al is het in zijn puurste vorm?
Waarom is gedestilleerd water niet geschikt om te drinken, ook al is het in zijn puurste vorm?  Nieuwe materialen helpen volumetrisch 3D-printen uit te breiden
Nieuwe materialen helpen volumetrisch 3D-printen uit te breiden Op ultraviolet licht gebaseerde coating is veelbelovend voor zelfdesinfecterende oppervlakken in medische instellingen, publieke ruimtes
Op ultraviolet licht gebaseerde coating is veelbelovend voor zelfdesinfecterende oppervlakken in medische instellingen, publieke ruimtes Waarom heeft natrium een hoger smeltpunt dan koper?
Waarom heeft natrium een hoger smeltpunt dan koper?  Wat is chloorfluorkoolwaterstof?
Wat is chloorfluorkoolwaterstof?
Hoofdlijnen
- Hoe worden obligaties gedefinieerd?
- Is er iemand? Menselijke embryo’s maken contact met aanstaande moeder
- Wanneer nakomelingen een mix van de ouders toont, is het ene allel dominant boven het andere?
- Wat is uniek aan de reproductie van Seahorse?
- Wetenschappers ontdekken hoe een bacteriële ziekteverwekker de barrières afbreekt om cellen binnen te dringen en te infecteren
- Verwijst naar het buitenoppervlak of de omgeving van een orgelstructuur?
- Nieuw inzicht in hoe de krachtcentrale van cellen zich deelt
- Mot bleek verschillende verdedigingsvloeistoffen af te scheiden om verschillende soorten roofdieren af te weren
- De geografische isolatie van twee populaties Een soort heeft de neiging om de verschillen tussen hun genenpools te vergroten omdat het?
- Onderzoekers ontdekken methode om kankerverwekkende formaldehydeafgifte uit hout in huis te beheersen

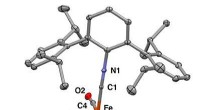
- Onstabiele molecuulklikken met synthetische strategie
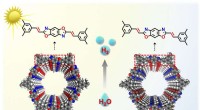
- Nieuwe isomere vinyleen-gekoppelde covalente organische raamwerken ontwikkeld met duidelijke fotokatalytische eigenschappen
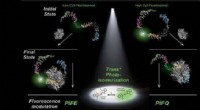
- Nieuwe experimentele inzichten stellen onderzoekers in staat eiwit-DNA-interacties met grotere precisie te onderzoeken
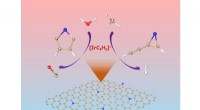
- Hoe twee isomeren van [IrC₄H₂]⁺ onafhankelijk reageren met methaan of water
 Hoeveel energie moet worden toegevoegd aan een glas van 2 kg met specifieke warmte 644 J kg verhoogt de temperatuur van 10oC 50OC?
Hoeveel energie moet worden toegevoegd aan een glas van 2 kg met specifieke warmte 644 J kg verhoogt de temperatuur van 10oC 50OC?  Welke factoren dragen bij aan academisch succes van studenten die in armoede leven?
Welke factoren dragen bij aan academisch succes van studenten die in armoede leven?  Over de mensen van de kustvlaktes
Over de mensen van de kustvlaktes  Biogas heeft geen subsidies nodig
Biogas heeft geen subsidies nodig Hoe Ampères te verhogen
Hoe Ampères te verhogen Effect van Photochemical Smog
Effect van Photochemical Smog  Twitter CEO zegt dat het bedrijf niet bevooroordeeld is, wil gezond debat
Twitter CEO zegt dat het bedrijf niet bevooroordeeld is, wil gezond debat Is de aarde tijdens haar baan altijd op dezelfde manier gekanteld?
Is de aarde tijdens haar baan altijd op dezelfde manier gekanteld?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

