
Wetenschap
Wat is de vorm van fosfor -trichloride?
* centraal atoom: Fosfor (P) is het centrale atoom.
* valentie -elektronen: Fosfor heeft 5 valentie -elektronen en elk chloor (CL) atoom heeft 7.
* binding: Fosfor vormt drie enkele covalente bindingen met drie chlooratomen.
* eenzaam paar: Fosfor heeft één eenzaam paar elektronen.
* Vorm: De vier elektronenparen rond fosfor rangschikken zichzelf in een tetraëdrische geometrie. Het enige paar oefent echter een sterkere afstoting uit dan de bindingsparen, waardoor de drie chlooratomen dichter bij elkaar worden geduwd, wat resulteert in een trigonale piramidale vorm.
Visuele weergave:
Stel je een piramide voor met een driehoekige basis, waarbij het fosforatoom zich aan de top bevindt en de drie chlooratomen zich aan de hoeken van de basis bevinden. Het enige paar op fosfor wijst naar beneden, waardoor het molecuul zijn piramidale vorm krijgt.
 Deskundigen stellen een langetermijnstrategie voor voor het risicobeheer van natuurbranden in het tijdperk van klimaatverandering
Deskundigen stellen een langetermijnstrategie voor voor het risicobeheer van natuurbranden in het tijdperk van klimaatverandering  VIIRS-satellietinstrument krijgt 2 keer de tropische cycloon Marcus
VIIRS-satellietinstrument krijgt 2 keer de tropische cycloon Marcus Closed-loop-concept kan de toekomst zijn van duurzame veehouderijen
Closed-loop-concept kan de toekomst zijn van duurzame veehouderijen Afbeelding:NASA's Aqua-satelliet legt rook vast die voor de kust van Californië opstookt
Afbeelding:NASA's Aqua-satelliet legt rook vast die voor de kust van Californië opstookt Wat is de natuur waard? Tel de selfies
Wat is de natuur waard? Tel de selfies
Hoofdlijnen
- Te veel voertuigen, trage reacties en roekeloos samenvoegen:nieuw wiskundig model legt uit hoe verkeersbacteriën bewegen
- Welk bioom bevindt zich in Canada en Rusland?
- Ocean meeting haalt meer dan $7 miljard op voor mariene bescherming
- Wat gebeurt er met aminozuren in levercellen?
- Hoe kan DNA worden gebruikt om de theorie te ondersteunen dat alle soorten een gemeenschappelijke afkomst delen?
- Waarom hitte gebruiken om de microbiële groei onder controle te houden?
- Weefsels regenereren met moleculen die gericht zijn op genen
- Wat hebben zeepbellen en vlinders met elkaar gemeen?
- Wat zit er in elke geslachtscel?
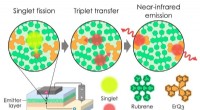
- Excitonlimieten zijn bedoeld om te worden overschreden:OLED overtreft 100 procent excitonproductie-efficiëntie
- 3D-printen verandert nanomachines in levensgrote arbeiders

- Wetenschappers stellen nieuwe selectieve reductieve aminekatalysatoren voor met verbeterde stabiliteit

- Een gel die niet breekt of uitdroogt

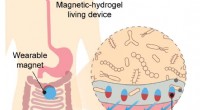
- Levende sensoren onderzoeken mysteries van de darm
 Welke chemicaliën worden gebruikt om drinkwater te zuiveren?
Welke chemicaliën worden gebruikt om drinkwater te zuiveren?  Het voortstuwingsteam van White Sands test een 3D-geprint Orion-motoronderdeel
Het voortstuwingsteam van White Sands test een 3D-geprint Orion-motoronderdeel  Noem en beschrijf het type tektonische spanning dat breuk- en blokkeerbergen vormt?
Noem en beschrijf het type tektonische spanning dat breuk- en blokkeerbergen vormt?  Hoe zijn koolstofstikstof en zuurstof vergelijkbaar?
Hoe zijn koolstofstikstof en zuurstof vergelijkbaar?  Review:Edifier koptelefoons en oordopjes geven je geweldig geluid, geen draden
Review:Edifier koptelefoons en oordopjes geven je geweldig geluid, geen draden Shine a light:nieuw onderzoek laat zien hoe energiezuinig licht plastic kan buigen
Shine a light:nieuw onderzoek laat zien hoe energiezuinig licht plastic kan buigen Zal een koude winter teken doden?
Zal een koude winter teken doden?  Amerikaanse rechtbank bevestigt gevaar van geluidskanonnen
Amerikaanse rechtbank bevestigt gevaar van geluidskanonnen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

