
Wetenschap
Hoeveel atomen zitten er in 63,5 g koolmonoxide?
De molmassa van koolmonoxide (CO) is 28,01 g/mol. Dit betekent dat één mol koolmonoxide 28,01 gram weegt.
Het getal van Avogadro is 6,022 x 10^23. Dit betekent dat één mol van welke stof dan ook 6,022 x 10^23 atomen (of moleculen) bevat.
Om het aantal atomen in 63,5 g koolmonoxide te berekenen, kunnen we dus de volgende formule gebruiken:
Aantal atomen =(massa in gram) / (molaire massa in g/mol) * getal van Avogadro
Als we de gegeven waarden in de formule vervangen, krijgen we:
Aantal atomen =(63,5 g) / (28,01 g/mol) * (6,022 x 10^23 atomen/mol)
Aantal atomen =1,43 x 10^24 atomen
Daarom zijn er 1,43 x 10^24 atomen in 63,5 g koolmonoxide.
 'Soundscapes' van eilanden laten potentieel zien voor het evalueren van het herstel van broedende zeevogels
'Soundscapes' van eilanden laten potentieel zien voor het evalueren van het herstel van broedende zeevogels  Injectieputten kunnen aardbevingen op kilometers afstand van de put veroorzaken
Injectieputten kunnen aardbevingen op kilometers afstand van de put veroorzaken Hoe op de natuur gebaseerde kennis lokale ecosystemen kan herstellen en het welzijn van de gemeenschap kan verbeteren
Hoe op de natuur gebaseerde kennis lokale ecosystemen kan herstellen en het welzijn van de gemeenschap kan verbeteren  Wat eet zeegras?
Wat eet zeegras?  Identificatie van witte vogeleieren
Identificatie van witte vogeleieren
Hoofdlijnen
- Hoeveel steenarenden zijn er?
- Mondiale meta-analyse kwantificeert de voordelen van het gebruik van bodembedekking
- Fysieke aanpassingen van rondwormen
- Hoe persistente bacteriën antibiotica kunnen vermijden
- Een dieper begrip van de seksuele ontwikkeling van malariaparasieten ontsluit mogelijkheden om de verspreiding van ziekten te blokkeren
- Vleermuizen zijn gastheer voor een reeks virussen, maar worden niet ziek. Waarom?
- Wat zijn enkele soorten bewijsmateriaal dat een forensisch botanicus verzamelt?
- Welke weefsels zorgen ervoor dat organen niet uit elkaar vallen?
- Waarom zijn planten groen? Het model van het onderzoeksteam reproduceert fotosynthese
- Goedkoop, efficiënte en stabiele foto-elektrode kan de watersplitsing met zonne-energie verbeteren

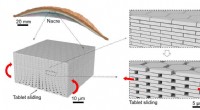
- Nieuw type glas geïnspireerd door de natuur is beter bestand tegen schokken
- Metaalschuim houdt kogels van .50 kaliber tegen, evenals staal - bij minder dan de helft van het gewicht

- Bouw van betere biosensoren in de gasfase voor de bestrijding van ziekten
- Het jaar voorspellen in de chemie

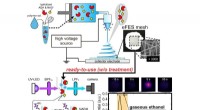
 Opgenomen nanodeeltjes kunnen de lever beschadigen
Opgenomen nanodeeltjes kunnen de lever beschadigen Hoe een wereldrecord 'squeeze' troost kan bieden voor jagers op donkere materie
Hoe een wereldrecord 'squeeze' troost kan bieden voor jagers op donkere materie  Zo snel terug, La Niña? Dit is de reden waarom we twee doorweekte zomers op rij krijgen
Zo snel terug, La Niña? Dit is de reden waarom we twee doorweekte zomers op rij krijgen  Koudwaterkoralen:verzuring schaadt, opwarming bevordert de groei
Koudwaterkoralen:verzuring schaadt, opwarming bevordert de groei Donkere halfgeleiders laten schitteren
Donkere halfgeleiders laten schitteren Opgeleide kinderen helpen vrouwen langer te leven, studie zegt:
Opgeleide kinderen helpen vrouwen langer te leven, studie zegt: Hoeveel botten zitten er in een lichaam?
Hoeveel botten zitten er in een lichaam?  Iran beveelt internetproviders Telegram te blokkeren
Iran beveelt internetproviders Telegram te blokkeren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

