
Wetenschap
Waarom vaste stoffen hebben alleen trillingsbeweging?
Dit is waarom:
* Sterke intermoleculaire krachten: Vaste stoffen hebben sterke intermoleculaire krachten (zoals ionische bindingen, covalente bindingen of metalen bindingen) die hun samenstellende deeltjes (atomen, ionen of moleculen) strak in een vaste, stijve structuur vasthouden. Deze sterke aantrekkingskracht beperkt de bewegingsvrijheid van deeltjes.
* Vaste posities: De deeltjes in een vaste bezette specifieke, goed gedefinieerde posities in de structuur. Ze kunnen niet vrij door de vaste stof bewegen zoals ze kunnen in vloeistoffen of gassen.
Dus, wat voor soort beweging hebben vaste stoffen?
* trillingsbeweging: De deeltjes in een vaste stof trillen constant rond hun vaste posities. Deze trillingen neemt toe met de temperatuur.
* Translationele beweging: Hoewel beperkt, hebben deeltjes in vaste stoffen een kleine hoeveelheid translationele beweging. Ze verschuiven enigszins rond hun vaste posities. Deze beweging is te klein om macroscopisch te worden waargenomen, maar is cruciaal voor het begrijpen van het gedrag van vaste stoffen, zoals hun thermische geleidbaarheid.
Waarom deze misvatting?
De misvatting kan voortkomen uit uitsluitend gericht op de macroscopische eigenschappen van vaste stoffen. Op macroscopisch niveau lijken vaste stoffen rigide en immobiel. Op microscopisch niveau zijn de deeltjes binnen een vaste stof echter constant in beweging, zij het beperkt en beperkt.
 Het belangrijkste product verkregen bij interactie van fenol met natriumhydroxide en koolstofdioxide is?
Het belangrijkste product verkregen bij interactie van fenol met natriumhydroxide en koolstofdioxide is?  Zou u natriumcarbonaat moeten gebruiken voor de diazotisatie van p-nitroaniline?
Zou u natriumcarbonaat moeten gebruiken voor de diazotisatie van p-nitroaniline?  Dierproeven vermijden met verbeterde methoden voor chemische risicobeoordeling
Dierproeven vermijden met verbeterde methoden voor chemische risicobeoordeling Ervoor zorgen dat orale geneesmiddelen worden beschermd tegen de zure omstandigheden van de maag
Ervoor zorgen dat orale geneesmiddelen worden beschermd tegen de zure omstandigheden van de maag Hoe metalliseert waterstof?
Hoe metalliseert waterstof?
Hoofdlijnen
- Hoe verdrijft een cel grote deeltjes?
- Wat zijn de huidige doelen van Human Genome Project?
- Wie bestudeert de Whater -cyclus?
- Hoe ziet de plant Pachysandra eruit?
- Wat geeft de afwezigheid van endosporen aan over een bacterie?
- Wat wordt het molecuul dat wordt gebruikt om gen uit DNA te snijden in een organisme?
- Nieuw wiskundig model onthult hoe grote groepen ontstaan in de evolutie
- Wat zijn chrysophytes?
- Een specifiek eiwit dat bepaalde moleculen herkent die ze over het membraan brengen?
- Bodemzware squirmers nemen kenmerkend groepsgedrag aan

- Energiebesparende servers:gegevensopslag 2.0
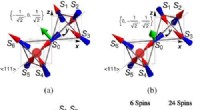
- Doorbraak in het begrijpen van magnetische monopolen kan wijzen op nieuwe technologieën
- Een nieuwe kwantumparadox zet de fundamenten van de waargenomen werkelijkheid in twijfel

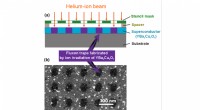
- Magnetische kwantumobjecten in een nano eierdoos
 Nieuwe tool ontworpen om de voedingsindustrie te helpen bij het stellen van doelstellingen voor klimaatverandering
Nieuwe tool ontworpen om de voedingsindustrie te helpen bij het stellen van doelstellingen voor klimaatverandering Hoe de 3D-structuur van ooglenseiwitten wordt gevormd
Hoe de 3D-structuur van ooglenseiwitten wordt gevormd  Hacker claimt inbreuk te maken op Uber, zegt beveiligingsonderzoeker
Hacker claimt inbreuk te maken op Uber, zegt beveiligingsonderzoeker Waarom heeft het zonnestelsel geen zwaartekracht?
Waarom heeft het zonnestelsel geen zwaartekracht?  Stadsgrootte speelt cruciale rol in migratiepatronen
Stadsgrootte speelt cruciale rol in migratiepatronen Welke kenmerken plaatsen mensen in dit koninkrijk?
Welke kenmerken plaatsen mensen in dit koninkrijk?  Biologisch materiaal verhoogt de prestaties van zonnecellen
Biologisch materiaal verhoogt de prestaties van zonnecellen Wat is een apparaat dat kracht of energie verzendt?
Wat is een apparaat dat kracht of energie verzendt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

