
Wetenschap
Ionische verbindingen een naam geven – Een duidelijke, stapsgewijze handleiding
ViktorCap/iStock/GettyImages
Ionische verbindingen een naam geven
Wanneer atomen elektronen delen, vormen ze covalente bindingen. Wanneer ionen met tegengestelde ladingen elkaar aantrekken, creëren ze ionische verbindingen die zichzelf rangschikken in een kristallijn rooster dat bekend staat als zout. Het benoemen van deze verbindingen gebeurt systematisch:identificeer eerst het kation (positief ion) en vervolgens het anion (negatief ion). Voor overgangsmetaalkationen wordt de oxidatietoestand aangegeven met Romeinse cijfers.
TL;DR
1. Eerst kationeren. 2. Anion tweede. 3. Voeg “‑ide” toe aan elementaire anionen. 4. Houd polyatomaire anionen ongewijzigd. 5. Geef voor overgangsmetalen de lading op in Romeinse cijfers.
Het kation komt op de eerste plaats
Het kation is het positief geladen ion, meestal een metaal. Elementen in Groepen 1 en 2 (alkali- en aardalkalimetalen) vormen ionen met vaste ladingen (respectievelijk 1+ en 2+). Een verbinding die natrium bevat, begint dus altijd met ‘natrium’ en een calciumverbinding begint met ‘calcium’.
Overgangsmetalen (Groepen 3–12) kunnen ionen vormen met meerdere oxidatietoestanden. De lading van het ion wordt tussen haakjes weergegeven achter de naam van het element. Bijvoorbeeld:
- Fe(III) – ferri-ijzer (Fe 3+ )
- Fe(II) – ferro-ijzer (Fe 2+ )
Het anion komt als volgende
Het anion is de negatief geladen soort. Het kan een enkel element zijn uit de groepen 15–17 of een polyatomair ion. Voor elementaire anionen wijzigt u de uitgang in “‑ide”:chloor → chloride, broom → bromide, zuurstof → oxide.
Gebruik voor polyatomaire anionen de gevestigde naam van het ion ongewijzigd. Voorbeelden:sulfaat (SO4 2‑ ), nitraat (NO3 ‑ ), carbonaat (CO3 2‑ ).
De lading van het kation bepalen op basis van de formule
Om een verbinding een naam te geven die een Groep1- of Groep2-kation bevat, schrijft u eenvoudigweg de kationnaam gevolgd door de anionnaam (indien nodig met het achtervoegsel “-ide”). Voorbeelden:natriumchloride, magnesiumsulfaat, calciumoxide.
Voor overgangsmetaalkationen wordt de oxidatietoestand afgeleid uit de algehele neutraliteit van de verbinding. Het subscript en de valentie van het anion begeleiden de berekening. Bijvoorbeeld:
- FeO:Oxide heeft een 2-lading; ijzer moet 2+ → ijzer(II)oxide zijn.
- Fe2 O3 :Twee oxiden (2×2‑ =4‑). Om in evenwicht te komen moet ijzer 3+ → ijzer(III)oxide zijn.
Het volgen van deze regels zorgt voor nauwkeurige, universeel geaccepteerde namen voor alle ionische verbindingen.
 Vijf jaar durende studie onthult hoeveel koolstof de ecologische hulpbronnen van China vastleggen
Vijf jaar durende studie onthult hoeveel koolstof de ecologische hulpbronnen van China vastleggen Wetenschappers detailleren onderzoek om de levensvatbaarheid en risico's van het ophelderen van mariene wolken te beoordelen
Wetenschappers detailleren onderzoek om de levensvatbaarheid en risico's van het ophelderen van mariene wolken te beoordelen  Spoedeisende atmosferische geo-engineering zou de oceanen niet redden
Spoedeisende atmosferische geo-engineering zou de oceanen niet redden  NC-eilanden mysterieuze geboorte verschijnt op NASA-satellietbeelden
NC-eilanden mysterieuze geboorte verschijnt op NASA-satellietbeelden Een goed leven voor iedereen binnen de planeten betekent
Een goed leven voor iedereen binnen de planeten betekent
Hoofdlijnen
- Wat is een hybride nakomelingen?
- Microbieel leven op Mars:zou zout water dit mogelijk kunnen maken?
- Zijn receptoren en enzymen beide in het celmembraan gelegen?
- Hoe gebruiken wetenschappers genetisch bewijs bij het classificeren van organisme?
- Hoe verschillen prokaryoten van de andere koninkrijken?
- In welk proces vouwt een deel van het celmembraan naar binnen en omringt moleculen om ze in cel te brengen?
- Hoe bidsprinkhaankreeften de wereld begrijpen
- Wat zijn de reproductieve bloemenorganen?
- Wat produceert chemiosmose en waar het gebeurt?
- Onderzoekers ontdekken dat sommige cidermakers onnodige suiker toevoegen

- De cruciale rol van de gram-per-mol-conversiefactor in de stoichiometrie

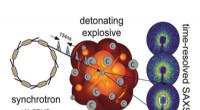
- Eerste Amerikaanse experimenten ooit in nieuwe röntgenfaciliteit kunnen leiden tot betere modellering van explosieven
- Video:De chemicaliën die we achterlaten

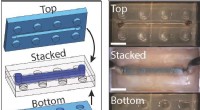
- Dynamische hydrogel die wordt gebruikt om zachte robotcomponenten en LEGO-achtige bouwstenen te maken
 Wat zijn de chemische samenstellingen van verschillende typen Feldspar?
Wat zijn de chemische samenstellingen van verschillende typen Feldspar?  Chinees ruimtevaartuig landt aan de andere kant van de maan
Chinees ruimtevaartuig landt aan de andere kant van de maan  Onderzoek naar de porositeit van sedimentair gesteente met neutronen
Onderzoek naar de porositeit van sedimentair gesteente met neutronen  Lijkt de massa van een planeten te beïnvloeden hoeveel manen deze heeft?
Lijkt de massa van een planeten te beïnvloeden hoeveel manen deze heeft?  Wat zijn functies boven de grond en onder de grond?
Wat zijn functies boven de grond en onder de grond?  Waarom blijft vast water drijven als het in vloeibaar water wordt geplaatst?
Waarom blijft vast water drijven als het in vloeibaar water wordt geplaatst?  Waarom moet je energie produceren energie?
Waarom moet je energie produceren energie?  Hoe kwetsbare metrosystemen te beschermen tegen terroristische aanslagen
Hoe kwetsbare metrosystemen te beschermen tegen terroristische aanslagen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

