
Wetenschap
Hoe concentratie de chemische reactiesnelheid beïnvloedt
ValentynVolkov/iStock/GettyImages
Hoe concentratie de reactiesnelheid stimuleert
Bij elke chemische transformatie wordt de snelheid waarmee producten worden gevormd bepaald door de frequentie van effectieve botsingen tussen reactantmoleculen. Door de concentratie van een reactant te verhogen, vergroot u de kans op een botsing, waardoor de reactie wordt versneld. Deze relatie is echter niet altijd lineair; bij hoge concentraties kan de reactie beperkt worden door factoren zoals diffusie of de beschikbaarheid van andere reactanten.
Botsingstheorie in de praktijk
De botsingstheorie voorspelt dat de snelheidsconstante k is evenredig met het aantal succesvolle botsingen. Wanneer alle reactanten in overmaat aanwezig zijn, volgt de snelheid de wet van massa-actie:r = k[A]^m[B]^n . Als er sprake is van een grote overmaat aan één component, kan de snelheid onafhankelijk van de concentratie lijken.
Voorbeelden uit de echte wereld
Magnesium en zoutzuur :Magnesiummetaal reageert met waterig HCl om waterstofgas te produceren. Een hogere HCl-concentratie levert meer H+ op ionen, waardoor de snelheid waarmee het metaal oplost toeneemt. Als magnesium overvloedig aanwezig is, heeft een verdere toename van HCl een afnemend effect.
Calciumcarbonaat en zoutzuur :Bij deze zuur-base-reactie stijgt de snelheid met de HCl-concentratie totdat het vaste carbonaat volledig is verbruikt. Het toevoegen van meer vast calciumcarbonaat voorbij dit punt versnelt het proces niet.
Enzymatische katalyse :Biologische reacties worden vaak gemedieerd door enzymen. De snelheid stijgt lineair met de enzymconcentratie totdat het substraat de beperkende factor wordt, waarna de reactie verzadiging bereikt.
Reactiepercentages meten
De meest directe aanpak is het monitoren van het verbruik van een reactant of het uiterlijk van een product in de loop van de tijd. Veel voorkomende technieken zijn onder meer gasverzameling, massaverandering, spectrofotometrie en calorimetrie. De waterstof die vrijkomt wanneer magnesium reageert met zuur kan bijvoorbeeld worden opgevangen in een maatcilinder, waardoor een duidelijk kinetisch profiel ontstaat.
Door de concentratie uit te zetten tegen de tijd, kan men bepalen of het veranderen van de concentratie van een reactant de helling verandert – een indicator voor snelheidsverandering. Dergelijke gegevens vormen de basis van de kwantitatieve chemie en worden routinematig gebruikt in onderzoek en industrie.
Bedenk dat de snelheid niet alleen door concentratie wordt beïnvloed; temperatuur, druk, katalysatoren en fysieke toestand spelen ook een cruciale rol.
 Wat is de structurele formule van een fosfaatradicaal?
Wat is de structurele formule van een fosfaatradicaal?  Kristallisatie begrijpen:een uitgebreide gids voor het proces
Kristallisatie begrijpen:een uitgebreide gids voor het proces  Is waterstof een geleider of isolator?
Is waterstof een geleider of isolator?  Onderzoek toont de rol aan van intra-mebrane interacties bij de beheersing van celdood door virussen
Onderzoek toont de rol aan van intra-mebrane interacties bij de beheersing van celdood door virussen Een veelbelovende oplossing om de hydrofobiciteit van het oppervlak van hydrofobe membranen te verbeteren
Een veelbelovende oplossing om de hydrofobiciteit van het oppervlak van hydrofobe membranen te verbeteren
 Mogelijk ontbreekt een sleutelfactor in modellen die uitbraken van ziekten door klimaatverandering voorspellen
Mogelijk ontbreekt een sleutelfactor in modellen die uitbraken van ziekten door klimaatverandering voorspellen Hoe beïnvloeden het leven van de verwering en erosie mensen?
Hoe beïnvloeden het leven van de verwering en erosie mensen?  Wat krijg je uit het bos?
Wat krijg je uit het bos?  Onderzoekers verzamelen nauwkeuriger weer, klimaatgegevens met behulp van onbemand luchtsysteem
Onderzoekers verzamelen nauwkeuriger weer, klimaatgegevens met behulp van onbemand luchtsysteem Zuid-Afrika om kolengestookte energie te verhogen, klimaatverontwaardiging aanwakkeren
Zuid-Afrika om kolengestookte energie te verhogen, klimaatverontwaardiging aanwakkeren
Hoofdlijnen
- Leuke organismen eindigen als eerste:waarom samenwerkers op de lange termijn altijd winnen
- Wat is het proces in een bepaald meercellig organisme waarmee speciale cellen nieuwe weefsels uit verschillende typen kunnen laten groeien?
- Wat is de intermembrale index van de mens?
- Hoe komt DDT in de lichamen van zoöplankton?
- DNA-onderzoek in de Stille Oceaan onthult een toename van 2000 procent in onze kennis van de biodiversiteit van weekdieren
- Wat zijn drie celorganellen die samenwerken?
- Endosymbiotische organellen:oorsprong, kenmerken en voorbeelden
- Noem twee kenmerken van levende organismen die hen onderscheiden van niet -levende dingen.
- Welk deel van het DNA wordt gekopieerd in eiwitsynthese?
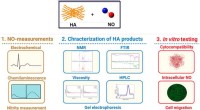
- Onderzoekers gebruiken stikstofmonoxidevangers om triple-negatieve borstkanker aan te pakken
- Nieuw ontdekte combinatie van koper en grafiet kan leiden tot efficiëntere lithium-ionbatterijen

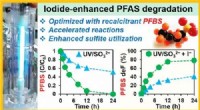
- PFAS-chemicaliën gaan niet eeuwig mee
- Diep-UV-sonderingsmethode detecteert elektronenoverdracht in fotovoltaïsche energie

- Materiaal voor nieuwe generatie atoomreactoren ontwikkeld

 Wat is de belangrijkste energiebron voor continentale drift?
Wat is de belangrijkste energiebron voor continentale drift?  Wat zijn basisschimmels geclassificeerd?
Wat zijn basisschimmels geclassificeerd?  Oproep tot paradigmaverschuiving om de verspreiding van COVID-19 door de lucht binnenshuis te bestrijden
Oproep tot paradigmaverschuiving om de verspreiding van COVID-19 door de lucht binnenshuis te bestrijden Hoe je Oscar-genomineerde films vanaf je bank kunt bekijken
Hoe je Oscar-genomineerde films vanaf je bank kunt bekijken  Een RAVAN in de zon
Een RAVAN in de zon Wat is het proces van een stof die energie afgeeft door elektromagnetische golven?
Wat is het proces van een stof die energie afgeeft door elektromagnetische golven?  Facebooks oproep tot wereldwijde internetregulering leidt tot debat
Facebooks oproep tot wereldwijde internetregulering leidt tot debat Hoe verhoudt thermodynamica zich tot energie en kracht?
Hoe verhoudt thermodynamica zich tot energie en kracht?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

