
Wetenschap
Het berekenen van het aantal mol van een chemische verbinding:een praktische gids
Door Michael Judge | Bijgewerkt op 30 augustus 2022
In de scheikunde is een mol de eenheid die de massa van een stof koppelt aan het aantal moleculen of atomen die de stof bevat. Eén mol is gelijk aan 6,022×10²³ entiteiten (het getal van Avogadro), waardoor het een essentieel hulpmiddel is voor kwantitatieve analyse.
Stap1 – Identificeer de molecuulformule
Begin met de exacte molecuulformule van de verbinding. De formule vertelt je hoeveel atomen van elk element aanwezig zijn in één molecuul. Water is bijvoorbeeld H₂O, wat betekent dat elk molecuul twee waterstofatomen en één zuurstofatoom bevat.
Stap2 – Atoomgewichten ophalen
Raadpleeg een periodiek systeem om het atoomgewicht (ook wel atoommassa genoemd) van elk element in de formule te vinden. Typische waarden zijn 1,008 g/mol voor waterstof en 16,00 g/mol voor zuurstof.
Stap3 – Bereken de molaire massa
Vermenigvuldig het atoomgewicht van elk element met het aantal atomen van dat element en tel de resultaten bij elkaar op:
(2×1,008)+(1×16,00)=18,016g/mol
Dit totaal, uitgedrukt in gram per mol, is de molaire massa van de verbinding.
Stap4 – Converteer massa naar mol
Deel de massa van het monster (in grammen) door de molaire massa om het aantal mol te verkrijgen:
25gH₂O 18,016 g/mol≈1,39 mol
Hulpmiddelen die je nodig hebt
- Periodiek systeem (gedrukt of digitaal)
- Wetenschappelijke rekenmachine
Volg deze stappen om het aantal mol voor elke chemische stof te berekenen, of je nu in een laboratorium werkt of scheikundecursussen studeert.
Het beheersen van molberekeningen ontgrendelt de mogelijkheid om nauwkeurige stoichiometrische berekeningen uit te voeren, experimenten te ontwerpen en analytische gegevens te interpreteren.
 Waar vloeistof de lucht ontmoet:ontdekken hoe luchtverontreinigende stoffen zich vormen
Waar vloeistof de lucht ontmoet:ontdekken hoe luchtverontreinigende stoffen zich vormen Onzichtbare barrière op oceaanoppervlak vermindert koolstofopname met de helft
Onzichtbare barrière op oceaanoppervlak vermindert koolstofopname met de helft Ansjovis eet plastic omdat het naar prooi ruikt
Ansjovis eet plastic omdat het naar prooi ruikt Saber-tooth Kittens waren groot uitgebeend
Saber-tooth Kittens waren groot uitgebeend  Lokale lockdowns zorgden voor snelle wereldwijde ozonreducties, NASA vindt
Lokale lockdowns zorgden voor snelle wereldwijde ozonreducties, NASA vindt
Hoofdlijnen
- Waarom kunnen twee vergelijkbare soorten niet dezelfde niche hebben?
- Wat wordt een term die wordt gebruikt om de invloeden van meerdere genen op gedrag te beschrijven?
- Waarom staat de mitochondrion bekend als krachtpatser van eukaryotische cel?
- Wat is een DNA -segment dat de informatie bevat die nodig is om geërfde eigenschappen een organisme uit te drukken?
- Wat betekent experiment in de wetenschap?
- Wat is een cel die geen kern heeft?
- Waarom wordt de cellen de basiseenheidsstructuur en de functie van het levende dingen genoemd?
- Stimuleer stereotypen consumentenaankopen bij organisaties met of zonder winstoogmerk?
- Gluconeogenese beschrijft de conversie van wat?
- Elektrochemische reductie van kooldioxide tot ethanol

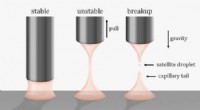
- Een nieuwe draai om visco-elastische vloeistofbruggen te doorbreken
- Bio-ingenieurs ontwikkelen zich snel, op speeksel gebaseerde detectietest voor marihuana

- Schoner maken, groenere kunststoffen uit afvalvisdelen

- Persistente versus niet-persistente chemicaliën:levensduur, toxiciteit en impact op het milieu

 Hoe helpen vulkanische rotsen planten te groeien?
Hoe helpen vulkanische rotsen planten te groeien?  Wat is het effect geweest van erosie in Ural Mountains?
Wat is het effect geweest van erosie in Ural Mountains?  Wat is de helderste planeet in het zonnestelsel?
Wat is de helderste planeet in het zonnestelsel?  Hoe bevordert chemische verwering mechanische verwering?
Hoe bevordert chemische verwering mechanische verwering?  Welke kracht wordt uitgeoefend tussen uw schoenen en de grond?
Welke kracht wordt uitgeoefend tussen uw schoenen en de grond?  Waarom vrouwen – inclusief feministen – zich nog steeds aangetrokken voelen tot 'welwillend seksistische' mannen
Waarom vrouwen – inclusief feministen – zich nog steeds aangetrokken voelen tot 'welwillend seksistische' mannen  Aanvulling van grondwater nauwkeuriger berekenen
Aanvulling van grondwater nauwkeuriger berekenen Fermilab-wetenschappers gaan op zoek naar donkere materie met behulp van kwantumtechnologie
Fermilab-wetenschappers gaan op zoek naar donkere materie met behulp van kwantumtechnologie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

