
Wetenschap
Hoe een calorimeter werkt:warmte meten in alledaagse experimenten
Door Claire Gillespie
Bijgewerkt op 30 augustus 2022
Анатолий Тушенцов/iStock/GettyImages
Een calorimeter klinkt misschien als een hightech gadget, maar het is een eenvoudig apparaat voor warmtemeting dat thuis kan worden gebouwd met twee koffiekopjes. Het wordt vaak gebruikt in wetenschapsprojecten op scholen en kwantificeert de energie die wordt uitgewisseld bij chemische of fysische processen, zoals warmteoverdracht of de soortelijke warmte van een stof.
TL;DR
Warmte zorgt ervoor dat de temperatuur van een vloeistof stijgt of daalt. Door de massa van de vloeistof en de resulterende temperatuurverandering te registreren, berekent een calorimeter de gewonnen of verloren energie.
Onderdelen van een calorimeter
Een basiscalorimeter bestaat uit twee vaten:een buitencontainer en een genest binnenvat. De lucht (of het schuim) daartussen fungeert als thermische isolator en voorkomt warmte-uitwisseling met de externe omgeving. Calorimeters van laboratoriumkwaliteit zijn vaak voorzien van een vezelring die het binnenvat gecentreerd houdt, een thermometer om de temperatuur te volgen en een roerder om de warmte gelijkmatig te verdelen. Een zelfgemaakte “koffiekopje”-versie is eenvoudiger maar minder nauwkeurig vanwege het grotere warmteverlies naar de omgeving.
Warmteoverdracht meten
Wanneer bij een exotherme reactie energie vrijkomt, stijgt de temperatuur van de oplossing; een endotherme reactie absorbeert energie, waardoor de temperatuur daalt. Door de temperatuurverschuiving samen met de soortelijke warmte en massa van de oplossing te meten, kunt u de warmteverandering van de reactie berekenen. Als u bijvoorbeeld een hete koperen staaf in een calorimeter in koud water steekt, stroomt er warmte van het koper naar het water totdat beide dezelfde temperatuur bereiken (thermisch evenwicht). Er verlaat geen warmte het systeem, dus alle overdracht vindt intern plaats.
Specifieke warmte meten
Soortelijke warmte is de hoeveelheid energie die nodig is om 1 gram van een stof met 1°C te laten stijgen. Het verschilt per materiaal. De soortelijke warmte van water is bijvoorbeeld 1,00 cal/g·°C. Om de soortelijke warmte van een onbekend metaal te bepalen, verwarm je het metaal en dompel je het vervolgens onder in water in het binnenvat. Noteer de uiteindelijke evenwichtstemperatuur. Bereken de warmte die door het water wordt geabsorbeerd (massa×soortelijke warmte×ΔT) en de warmte die verloren gaat door het metaal (massa×ΔT). Door de warmte van het water te delen door die van het metaal, ontstaat de soortelijke warmte van het metaal.
 Wetenschappers demonstreren met hoge resolutie dat lidar de geboortezone van wolkendruppeltjes ziet, een allereerste observatie op afstand
Wetenschappers demonstreren met hoge resolutie dat lidar de geboortezone van wolkendruppeltjes ziet, een allereerste observatie op afstand  Ontwikkelingslanden moeten hun eigen koers uitstippelen naar netto nulemissie
Ontwikkelingslanden moeten hun eigen koers uitstippelen naar netto nulemissie Filippijnse dorpelingen zetten zich schrap terwijl vulkaan onrustig wordt
Filippijnse dorpelingen zetten zich schrap terwijl vulkaan onrustig wordt Conflictvervuiling, aangespoelde landmijnen en militaire emissies:hoe oorlog het milieu vernielt
Conflictvervuiling, aangespoelde landmijnen en militaire emissies:hoe oorlog het milieu vernielt  Is het mechanisme dat soorten in de loop van de tijd veranderde?
Is het mechanisme dat soorten in de loop van de tijd veranderde?
Hoofdlijnen
- De atoomkern begrijpen:protonen, neutronen en isotopen
- Wat is neurotransmitter en geef voorbeelden?
- Waarom zijn membraaneiwitten nodig voor actief transport?
- Wat is een organisme dat voedsel maakt door fotosynthese?
- Mondiale meta-analyse kwantificeert de voordelen van het gebruik van bodembedekking
- Wat zijn twee belangrijke soorten cellen die nerveus weefsel vormen?
- Wat is de onderlinge relatie in het metabolisme van koolhydraten en lipiden -eiwitten?
- Een spiercel maakt voedsel of stuurt berichten rond het lichaam is als een plant het een dierencel?
- Wie ontdekte orgel?
- Beheersing van equivalente gewichtsberekeningen:een uitgebreide gids

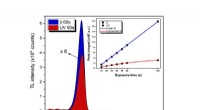
- Aluminiumoxidekristal getest als UV-stralingssensor
- Omgekeerde brandstofcel zet afvalkoolstof in recordtempo om in waardevolle producten

- Onderzoekers zetten AI aan het werk bij het maken van scheikundige voorspellingen

- Het ABS van moleculaire motoren

 Wat vertegenwoordigen de blokken in Feynman -lezing over energie?
Wat vertegenwoordigen de blokken in Feynman -lezing over energie?  Welk lichaamsdeel heeft 9 delen?
Welk lichaamsdeel heeft 9 delen?  Welke windenerosie wordt ervoor gezorgd dat zandkorrels piteren en poetsen wanneer ze ze raakten?
Welke windenerosie wordt ervoor gezorgd dat zandkorrels piteren en poetsen wanneer ze ze raakten?  Welke energie uit het zwembad is nodig om een golf te vormen en waar kwam vandaan?
Welke energie uit het zwembad is nodig om een golf te vormen en waar kwam vandaan?  Welke kleine stukjes gesteente of stof die de zon orbit worden genoemd?
Welke kleine stukjes gesteente of stof die de zon orbit worden genoemd?  Ontwikkeling van de zon:superbloei of superbuste voor woestijnsoorten?
Ontwikkeling van de zon:superbloei of superbuste voor woestijnsoorten?  Kunnen avatars de manier veranderen waarop we denken en handelen? (met video)
Kunnen avatars de manier veranderen waarop we denken en handelen? (met video)  Van de natuur afgeleide peptiden als moleculaire hulpmiddelen om cellulaire signalering te bestuderen
Van de natuur afgeleide peptiden als moleculaire hulpmiddelen om cellulaire signalering te bestuderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

