
Wetenschap
Inzicht in waterstof in reductiereacties:winst of verlies?
Hier is een overzicht van waarom:
* Reductie wordt gedefinieerd als de winst van elektronen.
* Waterstof kan op twee manieren betrokken zijn bij reductie:
* Verlies van waterstof: Bij sommige reacties betekent de verwijdering van waterstofatomen (of protonen, H+) uit een molecuul reductie. Dit is typisch in de organische chemie, waar reductie vaak de toevoeging van waterstof aan een dubbele of drievoudige binding inhoudt.
* Winst van waterstof: In andere gevallen kan reductie de *toevoeging* van waterstofatomen aan een molecuul inhouden. Dit gebeurt vaak wanneer een metaalion elektronen verkrijgt en waterstofionen (H+) worden gereduceerd tot waterstofgas (H₂).
Voorbeelden:
* Verlies van waterstof: De reductie van een aldehyde tot een alcohol omvat de toevoeging van twee waterstofatomen (H+) aan de carbonylgroep. Dit is een klassiek voorbeeld van reductie waarbij waterstof wordt gewonnen.
* Winst van waterstof: De reductie van een metaalion, zoals Fe³⁺ tot Fe²⁺, kan plaatsvinden in aanwezigheid van waterstofgas. De waterstof wordt geoxideerd tot H+, terwijl het metaalion elektronen krijgt.
Belangrijkste punten:
* Reductie gaat over de winst van elektronen, niet noodzakelijkerwijs over het verlies of de winst van waterstof.
* De specifieke chemische reactie bepaalt of waterstof verloren gaat of gewonnen wordt tijdens de reductie.
Laat het me weten als je nog vragen hebt!
 Wat zijn de ingrediënten voor verbranding?
Wat zijn de ingrediënten voor verbranding?  Wat is de formule voor één bariumatoom om de twee fluoratomen?
Wat is de formule voor één bariumatoom om de twee fluoratomen?  Onderzoekers lossen het mysterie op van hoe gasbellen in vloeistof ontstaan
Onderzoekers lossen het mysterie op van hoe gasbellen in vloeistof ontstaan  Het gebruik van koolwaterstofgas
Het gebruik van koolwaterstofgas  Onderzoekers ontdekken een nieuw bindingsmechanisme tussen kleine en gigantische deeltjes
Onderzoekers ontdekken een nieuw bindingsmechanisme tussen kleine en gigantische deeltjes
 Lessen uit een natuurbrand over hoe je de levens van huisdieren kunt redden
Lessen uit een natuurbrand over hoe je de levens van huisdieren kunt redden  Caltech krijgt een toezegging van $ 750 miljoen voor duurzaamheidsonderzoek
Caltech krijgt een toezegging van $ 750 miljoen voor duurzaamheidsonderzoek Ondanks wat je misschien hoort, worden de weersvoorspellingen beter, niet slechter
Ondanks wat je misschien hoort, worden de weersvoorspellingen beter, niet slechter  Experts verklaren het effect van klimaatverandering op infrastructuur
Experts verklaren het effect van klimaatverandering op infrastructuur Hebben onderzoekers de ontbrekende schakel gevonden die het mysterieuze fenomeen verklaart dat bekend staat als sprookjescirkels?
Hebben onderzoekers de ontbrekende schakel gevonden die het mysterieuze fenomeen verklaart dat bekend staat als sprookjescirkels?
Hoofdlijnen
- Overgewicht? Haal de darmbacteriën van iemand anders
- De informatie in DNA is wat bevat?
- Welke soorten wetenschapper bestudeert ziekteverwekkers?
- Waar verwijst osmose naar?
- Hoe heet het membraan dat de ene cel van de andere scheidt?
- Welke drie organellen hebben DNA?
- Je vindt een soort cel die je nog nooit eerder hebt gezien. Het heeft zowel kern als muur. Concludeer daarom dat het cel moet zijn.
- Omdat een membraan bestaat uit twee of meer soorten tissues, is het een voorbeeld a?
- Walvisclans gebruiken vocalisaties om hun cultuur te markeren
- Hoe bacteriën edelmetalen kunnen terugwinnen uit batterijen van elektrische voertuigen

- Monolithische nanokoolstofkatalysatoren starten selectieve oxidatie van diwaterstofsulfide

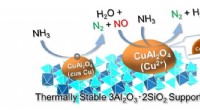
- Nieuwe katalysator maakt van ammoniak een innovatieve schone brandstof
- Rood, wit maar zelden blauw - de wetenschap van vuurwerkkleuren, uitgelegd

- Polyamiden van terpenen:Amorf Caramid-R en semi-kristallijn Caramid-S

 Hoe verschillend Zodiac Constellations verschillen van andere in de nachtelijke hemel?
Hoe verschillend Zodiac Constellations verschillen van andere in de nachtelijke hemel?  Het menselijke been:een uitgebreid overzicht van botten, spieren en gewrichten
Het menselijke been:een uitgebreid overzicht van botten, spieren en gewrichten  Wat moet waar zijn als eencellige organismen in het domein eukarya zijn geëvolueerd?
Wat moet waar zijn als eencellige organismen in het domein eukarya zijn geëvolueerd?  NASA stelt composiet samen van tropische storm Kong-Rey
NASA stelt composiet samen van tropische storm Kong-Rey Wat eten Angelfish in het wild?
Wat eten Angelfish in het wild?  Door licht aangedreven genezing van een draagbare elektrische geleider
Door licht aangedreven genezing van een draagbare elektrische geleider Wat gebeurt er als de zon over denkbeeldige lijn is?
Wat gebeurt er als de zon over denkbeeldige lijn is?  Wat zijn de variëteiten van steenkool gevormd in de aarde?
Wat zijn de variëteiten van steenkool gevormd in de aarde?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

