
Wetenschap
BH3 Lewis-structuur:overtreding van de Octet-regel uitgelegd
Ja, de Lewis-structuur van BH3 bevat een atoom dat niet aan de octetregel voldoet.
Dit is waarom:
* Boor (B) heeft slechts 3 valentie-elektronen.
* In BH3 vormt boor drie enkelvoudige bindingen met drie waterstofatomen. Dit maakt gebruik van alle drie de valentie-elektronen van boor.
* Boor heeft slechts 6 elektronen in zijn valentieschil. Dit is minder dan de 8 elektronen die nodig zijn om aan de octetregel te voldoen.
Daarom is boor in BH3 een voorbeeld van een atoom dat niet aan de octetregel voldoet. Er wordt feitelijk aangenomen dat het elektronentekort heeft .
Dit is een gemeenschappelijk kenmerk van boorverbindingen en draagt bij aan hun unieke reactiviteit.
 Wat is de omgekeerde vergelijking van lichte reacties?
Wat is de omgekeerde vergelijking van lichte reacties?  Dalian coherente lichtbron onthult zuurstofproductie door drie-lichamen fotodissociatie van water
Dalian coherente lichtbron onthult zuurstofproductie door drie-lichamen fotodissociatie van water Nieuw materiaal biedt milieuvriendelijke oplossing om restwarmte om te zetten in energie
Nieuw materiaal biedt milieuvriendelijke oplossing om restwarmte om te zetten in energie Heeft temperatuur atomen en moleculen?
Heeft temperatuur atomen en moleculen?  Hoe heet benzeen met een NH2-groep?
Hoe heet benzeen met een NH2-groep?
 Verband tussen continentaal uiteenvallen, vulkanische koolstofemissies en evolutie
Verband tussen continentaal uiteenvallen, vulkanische koolstofemissies en evolutie Studie vindt stijgende ozon een verborgen bedreiging voor maïs
Studie vindt stijgende ozon een verborgen bedreiging voor maïs Hoe bosbranden drinkwaterbronnen vervuilen
Hoe bosbranden drinkwaterbronnen vervuilen  Onderzoekers schetsen visie voor winstgevende oplossing voor klimaatverandering
Onderzoekers schetsen visie voor winstgevende oplossing voor klimaatverandering Hoe de eenvoudige houtsnippers wereldwijd water opruimen
Hoe de eenvoudige houtsnippers wereldwijd water opruimen
Hoofdlijnen
- Het proces door welke cel verdeelt om twee nieuwe cellen te vormen wordt genoemd?
- De donkergekleurde ronde structuur in de kern staat bekend als?
- Naar welk gezin behoort Beryllium?
- Een dier trainen? Een ethicus legt uit hoe en waarom jouw hond, maar niet de kikker, gestraft kan worden
- Noem de Tubluar -klieren die worden gevonden tussen bases van darmvilli?
- Waar bestaat de darmflora voornamelijk uit?
- Is Yellow Fever -virus DNA of RNA?
- 'Vliegende vaccinator':kunnen genetisch gemanipuleerde muggen een nieuwe strategie tegen malaria bieden?
- Aseksuele cellen:definitie, reproductie en voorbeelden
- Een kankervernietigersubstantie met nieuw werkingsmechanisme gevonden

- Lasergekoelde ionen dragen bij aan een beter begrip van wrijving
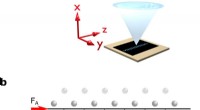
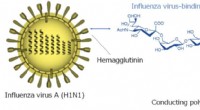
- Een bliksemsnelle griepvirusdetector
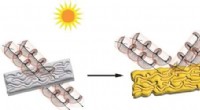
- Licht op waarom plastic geel wordt
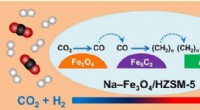
- Wetenschappers ontwikkelen efficiënte multifunctionele katalysator voor CO2-hydrogenering tot benzine
 Wetenschappers ontdekken nieuwe manier om ruimtevaartuigfouten te voorkomen
Wetenschappers ontdekken nieuwe manier om ruimtevaartuigfouten te voorkomen Hoe wordt geometrie in het echte leven gebruikt?
Hoe wordt geometrie in het echte leven gebruikt?  Waarom zijn zowel elektronen als water en water?
Waarom zijn zowel elektronen als water en water?  Welke verbinding maakt aluminium broom en zuurstof?
Welke verbinding maakt aluminium broom en zuurstof?  Wat gebeurt er als de scheurde limoen reageert met chloor?
Wat gebeurt er als de scheurde limoen reageert met chloor?  Terwijl de klimaatverandering de permafrost van Alaska doet smelten, wegen zinken, bruggen kantelen en broeikasgassen komen vrij
Terwijl de klimaatverandering de permafrost van Alaska doet smelten, wegen zinken, bruggen kantelen en broeikasgassen komen vrij Sparen of uitgeven? Advertentiebeslissingen te midden van mond-tot-mondreclame door consumenten
Sparen of uitgeven? Advertentiebeslissingen te midden van mond-tot-mondreclame door consumenten  'S Werelds eerste bloedtest voor realtime monitoring van het succes van kankerbehandelingen
'S Werelds eerste bloedtest voor realtime monitoring van het succes van kankerbehandelingen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

