
Wetenschap
Arrhenius-zuren en basen:definities en voorbeelden
Zuren:
* Produceer waterstofionen (H+) wanneer opgelost in water.
*Dit betekent dat ze de concentratie H+-ionen in de oplossing verhogen.
Basis:
* Produceer hydroxide-ionen (OH-) wanneer opgelost in water.
*Dit betekent dat ze de concentratie OH-ionen in de oplossing verhogen.
Hier zijn enkele voorbeelden:
Zuren:
* Zoutzuur (HCl): HCl → H+ + Cl-
* Salpeterzuur (HNO3): HNO3 → H+ + NO3-
* Zwavelzuur (H2SO4): H2SO4 → 2H+ + SO42-
Basis:
* Natriumhydroxide (NaOH): NaOH → Na+ + OH-
* Kaliumhydroxide (KOH): KOH → K+ + OH-
* Calciumhydroxide (Ca(OH)2): Ca(OH)2 → Ca2+ + 2OH-
Belangrijke punten om te onthouden over de Arrhenius-theorie:
* Het richt zich op het gedrag van zuren en basen in waterige oplossingen.
* Het is een eenvoudig en nuttig model om de eigenschappen van zuren en basen te begrijpen, maar het heeft beperkingen.
* Het verklaart niet het gedrag van stoffen die werken als zuren of basen in niet-waterige oplosmiddelen.
Laat het me weten als je meer wilt weten over andere zuur-base-theorieën zoals Brønsted-Lowry of Lewis!
 Wat is de reactie die directe energie van zonlicht vereist om dragermoleculen te maken?
Wat is de reactie die directe energie van zonlicht vereist om dragermoleculen te maken?  Hoe worden elektronen uit atomen verwijderd om ionen in een massaspectrometer te vormen?
Hoe worden elektronen uit atomen verwijderd om ionen in een massaspectrometer te vormen?  Is dichtheid een chemische eigenschap van materie?
Is dichtheid een chemische eigenschap van materie?  Waarom heeft een thermosfles verzilverd glas en vacuüm?
Waarom heeft een thermosfles verzilverd glas en vacuüm?  In een molecuul van stikstof worden drie paren elektronen gedeeld door twee atomen, de type binding die wordt gevormd als een voorbeeld an?
In een molecuul van stikstof worden drie paren elektronen gedeeld door twee atomen, de type binding die wordt gevormd als een voorbeeld an?
Hoofdlijnen
- Wat doen de ribosomen voor dierencel?
- Een organisme met twee als genen voor een triat wordt genoemd wat die eigenschap?
- Er bestaat een eiwitmolecuul op?
- Studie ontdekt hoe sommige eencellige organismen microbiomen controleren
- Waarom mensen schreeuwen en gekke gezichten trekken als ze doodsbang zijn
- Een dierencel die omringd door zoet water zal barsten omdat osmose veroorzaakt?
- Het proces van cellen die samen klonten staat bekend als?
- Hoe varens en paddenstoelen reproduceren?
- Wat is superieur DNA?
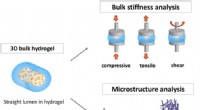
- Semi-flexibele modelgebaseerde analyse van celadhesie aan hydrogels
- Onderzoekers ontwerpen nieuwe moleculen die de brandstofefficiëntie verhogen

- Onderzoekers vinden potentieel gebruik voor gerecycled plastic in beton

- Vrijstaande microwire-array maakt flexibel zonnevenster mogelijk

- Biovriendelijke protocellen pompen bloedvaten op

 Wat is het effect van HCl op verbrande en onverbrande Mg-strips?
Wat is het effect van HCl op verbrande en onverbrande Mg-strips?  Onderzoekers ID veelbelovende sleutel tot prestaties van elektronica van de volgende generatie
Onderzoekers ID veelbelovende sleutel tot prestaties van elektronica van de volgende generatie De evenwichtsconstante voor de onderstaande reactie is 0,49 bij O2 is gelijk aan 0,11 en N2 0,15 Welke concentratie NEE?
De evenwichtsconstante voor de onderstaande reactie is 0,49 bij O2 is gelijk aan 0,11 en N2 0,15 Welke concentratie NEE?  In welk jaar werd elke planeet in uw zonnestelsel ontdekt?
In welk jaar werd elke planeet in uw zonnestelsel ontdekt?  Deze 6 nieuwe SUV's zijn het wachten waard
Deze 6 nieuwe SUV's zijn het wachten waard Waarom zijn er geen wettelijke beschermingen voor de kinderen van influencers?
Waarom zijn er geen wettelijke beschermingen voor de kinderen van influencers?  Kwantumsprong in AI-gerelateerde octrooiaanvragen:VN (update)
Kwantumsprong in AI-gerelateerde octrooiaanvragen:VN (update) Aardwetenschappen, wat is tot?
Aardwetenschappen, wat is tot?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

