
Wetenschap
Berekening van het aantal xenonatomen bij STP:een stapsgewijze handleiding
1. Gebruik de ideale gaswet:
De ideale gaswet is:PV =nRT
* P =Druk (in atm)
* V =Volume (in liters)
* n =Aantal mol
* R =Ideale gasconstante (0,0821 L·atm/mol·K)
* T =Temperatuur (in Kelvin)
2. Bepaal de voorwaarden bij STP:
* STP (standaardtemperatuur en druk) wordt gedefinieerd als:
* Temperatuur:0°C =273,15 K
* Druk:1 atm
3. Bereken het aantal mol (n):
* Sluit de waarden aan op de ideale gaswet:
(1 atm) * (10,0 L) =n * (0,0821 L·atm/mol·K) * (273,15 K)
* Los op voor n:
n =(1 atm * 10,0 L) / (0,0821 L·atm/mol·K * 273,15 K) ≈ 0,446 mol Xe
4. Converteer mollen naar atomen:
* Gebruik het getal van Avogadro (6,022 x 10^23 atomen/mol) om mollen in atomen om te zetten:
0,446 mol Xe * (6,022 x 10^23 atomen/mol) ≈ 2,68 x 10^23 Xe atomen
Daarom zijn er bij STP ongeveer 2,68 x 10^23 xenonatomen in 10,0 liter Xe-gas.
 Kun je zuurstofbleekmiddel en ammoniak mengen?
Kun je zuurstofbleekmiddel en ammoniak mengen?  Als ethylbenzoaat gebruikte om trifenylmethanol te bereiden, is nat wat bijproduct is gevormd?
Als ethylbenzoaat gebruikte om trifenylmethanol te bereiden, is nat wat bijproduct is gevormd?  Wat zijn de gram molecuulgewichten van C6H8O7?
Wat zijn de gram molecuulgewichten van C6H8O7?  Hoe kunnen chloorniveaus 0 tot donker oranje registreren met de toevoeging van een beetje vloeibaar chloor?
Hoe kunnen chloorniveaus 0 tot donker oranje registreren met de toevoeging van een beetje vloeibaar chloor?  Verschil tussen Nylon 6 en Nylon 66
Verschil tussen Nylon 6 en Nylon 66
Hoofdlijnen
- Wat is een biofonie?
- Onderzoek naar de effectiviteit van methoden om onvoorziene beworteling van Lindera-benzoëstengelstekken te stimuleren
- Welke van de volgende structuren worden aangetroffen in eukaryotische cellen maar geen prokaryotische cellen?
- Welk organisme kan veranderen van autotrofe naar heterotrofe?
- Waarom is een atom elektrisch neutraal?
- Wat zijn de kleinste structuren die biologen beschouwen als leven?
- Wat zijn de takken van microbiologie?
- Wat is stratocumclus?
- Is de celmeembraan in staat chemische signalen te ontvangen en te herkennen?
- Autonoom groeiende synthetische DNA-strengen

- Stabiele radicalen kunnen onconventionele problemen in de moderne wetenschap en technologie oplossen

- Op lipiden gebaseerde grensgesmeerde hydrogels bleken gladder te zijn dan die op basis van water
- Het periodiek systeem 180 graden draaien voor een nieuw perspectief
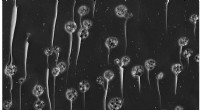
- Ingebedde druppelafdruktechnologie print en verwerkt druppeltjes die op hun plaats zijn opgehangen, gecontroleerd en verwerkt

 Wat zijn de grote landmassa in oceanen?
Wat zijn de grote landmassa in oceanen?  Wat in microbiële biomassa?
Wat in microbiële biomassa?  De wetenschap achter bakken:belangrijke chemische reacties uitgelegd
De wetenschap achter bakken:belangrijke chemische reacties uitgelegd  Hebben rode sterren hogere oppervlaktetemperaturen dan blauwe sterren?
Hebben rode sterren hogere oppervlaktetemperaturen dan blauwe sterren?  Zwaveldifluoride -ionische of covalente binding?
Zwaveldifluoride -ionische of covalente binding?  Sri Lanka beveelt teruggave van gesmokkeld Brits afval
Sri Lanka beveelt teruggave van gesmokkeld Brits afval Wat is het proces waarmee een cel chromosomen dupliceert en zich in twee cellen splitst?
Wat is het proces waarmee een cel chromosomen dupliceert en zich in twee cellen splitst?  Hoe Grams in Moleculen om te zetten
Hoe Grams in Moleculen om te zetten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

