
Wetenschap
Zuurstof en chemische stabiliteit:hoe verbindingen zuurstofatomen beïnvloeden
* Octetregel: Zuurstof heeft zes elektronen in de buitenste schil. Het wil acht elektronen hebben (zoals de edelgassen) om een stabiele configuratie te bereiken.
* Elektronen delen of verkrijgen: Om deze stabiliteit te bereiken, kan zuurstof:
* Delen twee elektronen met een ander atoom (die covalente bindingen vormen).
* Winst twee elektronen van een ander atoom (die ionische bindingen vormen).
* Stabiliteit: Door elektronen te delen of te verwerven, voltooit zuurstof zijn buitenste schil en wordt stabieler.
Voorbeelden:
* Water (H₂O): Zuurstof deelt twee elektronen met twee waterstofatomen en vormt stabiele covalente bindingen.
* Calciumoxide (CaO): Zuurstof haalt twee elektronen uit calcium en vormt zo een stabiele ionische binding.
Samengevat: Zuurstofatomen zijn zeer reactief in hun elementaire vorm. Door verbindingen te vormen, bereiken ze een stabielere elektronische configuratie, die voldoet aan de octetregel.
 Wetenschappers creëren een liefdesmolecuul met minder complicaties
Wetenschappers creëren een liefdesmolecuul met minder complicaties Een deeltje in de kern van een atoom?
Een deeltje in de kern van een atoom?  Wat is de zuur-basereactie voor HNO3 plus NaOH?
Wat is de zuur-basereactie voor HNO3 plus NaOH?  Nieuwe solid-state thermische diode ontwikkeld met betere rectificatieprestaties
Nieuwe solid-state thermische diode ontwikkeld met betere rectificatieprestaties Wat zijn de elektronendrager -moleculen van stoepranden cyle en kalvin -cyclus?
Wat zijn de elektronendrager -moleculen van stoepranden cyle en kalvin -cyclus?
Hoofdlijnen
- Wat zijn niet-fotosynthetisch?
- Wat eet andere cellen?
- Celdeling:groei, herstel en ontwikkeling - een uitgebreid overzicht
- Hoe slim zijn orka's? Orka's hebben de op één na grootste hersenen van alle zeezoogdieren
- Hoe elektrische vissen elektrische orgels konden ontwikkelen
- Wat is tamme gist?
- Niet alle dieren in het wild zijn hersteld in lockdowns, zo blijkt uit nieuw onderzoek
- Wat is het proces van het vormen van RNA uit DNA?
- Wat zou de complementaire DNA zijn voor sequentie CTTAGGCTTACCA?
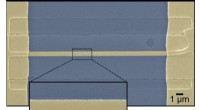
- Grenzen geen barrière voor thermo-elektriciteit
- Het produceren van ethaan uit methaan met behulp van een fotochemische lusstrategie

- Zelfassemblage van polypeptiden geleid door toevoeging van co-oplosmiddelen

- Onderzoekers ontwikkelen computermodel om te voorspellen of een bestrijdingsmiddel schadelijk is voor bijen

- Alcoholen vertonen kwantumeffecten
 Loden leidingen veilig maken
Loden leidingen veilig maken Welk lichaamssysteem is verantwoordelijk voor de reproductie?
Welk lichaamssysteem is verantwoordelijk voor de reproductie?  Wat zijn genen die geen onafhankelijk assortiment ondergaan?
Wat zijn genen die geen onafhankelijk assortiment ondergaan?  Lava morst uit Filippijnse vulkaan, as coating land
Lava morst uit Filippijnse vulkaan, as coating land Wat gebeurt er met een ballenkinetische energie als je de bal twee keer zo snel gooit?
Wat gebeurt er met een ballenkinetische energie als je de bal twee keer zo snel gooit?  CH3CH2CHCHCH3 begrijpen:is het penteen of pentaan?
CH3CH2CHCHCH3 begrijpen:is het penteen of pentaan?  Indringende vraag:Wat is het verschil tussen kikkers en padden?
Indringende vraag:Wat is het verschil tussen kikkers en padden?  Wat moeten watermoleculen winnen om te verdampen van vloeibaar water?
Wat moeten watermoleculen winnen om te verdampen van vloeibaar water?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

